
Componenti della via extrapiramidale, funzione, via, malattie

La nozione di approccio extrapiramidale o il sistema extrapiramidale (SEP) è nato a seguito di studi anatomici e fisiologici volti a comprendere il modo in cui il sistema nervoso centrale controllava l'attività dei muscoli scheletrici, con l'obiettivo che il corpo assumesse la postura corporea appropriata e producesse la movimenti.
In questo processo, si è scoperto che il controllo dell'attività muscolare richiedeva il controllo dei motoneuroni del corno anteriore del midollo spinale, l'unico collegamento tra il sistema nervoso centrale e le fibre muscolari scheletriche, e che questo controllo era esercitato dalle proiezioni nervose dai centri cerebrali superiori.
Tra queste proiezioni, un importante percorso è formato da alcuni assoni che hanno origine nelle aree motorie della corteccia cerebrale e scendono direttamente, cioè senza squame, al midollo spinale, unendosi, mentre passano attraverso il midollo allungato, in alcune prominenze a cui per la loro forma venne dato il nome di "piramidi".
Questo tratto era chiamato “tratto piramidale” o “tratto corticospinale” ed era coinvolto nel controllo dei movimenti fini e abili eseguiti dalle porzioni distali degli arti, mentre era riconosciuta ma non inclusa l'esistenza di strutture con funzione motoria. in questo modo (extra).
Il termine “sistema motorio extrapiramidale”, già obsoleto dal punto di vista fisiologico, è ancora utilizzato in gergo clinico per riferirsi a quelle strutture del cervello e del tronco encefalico che collaborano al controllo motorio, ma non fanno parte del sistema piramidale o corticospinale diretto.
Indice articolo
- 1 Componenti anatomiche e funzione della via piramidale
- 1.1 - Nuclei del tronco cerebrale
- 1.2 - Gangli della base
- 1.3 - Connettività, pathway e neurochimica nei gangli della base
- 2 Malattie dei gangli della base
- 2.1 Malattia di Huntington
- 2.2 Emibalismo
- 2.3 Morbo di Parkinson
- 3 Riferimenti
Componenti anatomiche e funzione della via piramidale
Il percorso extrapiramidale può essere descritto come organizzato in due gruppi di componenti: uno sarebbe costituito da un insieme di nuclei del tronco cerebrale e le sue proiezioni verso il midollo spinale, e l'altro sarebbe costituito dai nuclei sottocorticali noti come nuclei o gangli della base..
- Nuclei del tronco cerebrale
Nel tronco cerebrale ci sono gruppi di neuroni i cui assoni si proiettano verso la materia grigia del midollo spinale e che sono stati descritti come organizzati in due sistemi: uno mediale e l'altro laterale..
Sistema mediale
Il sistema mediale è formato dai tratti vestibolospinale, reticolospinale e tettospinale che scendono attraverso le corde ventrali del midollo ed esercitano il controllo sui muscoli assiali o del tronco, oltre ai muscoli prossimali delle estremità coinvolte nella postura del corpo..
Sistema laterale
La componente più importante del sistema laterale è il tratto rubrospinale, i cui assoni sporgono dal nucleo rosso del mesencefalo, scendono attraverso il midollo laterale del midollo e finiscono per influenzare i motoneuroni che controllano i muscoli distali delle estremità..
Da quanto precede si può dedurre che il sistema mediale collabora agli aggiustamenti posturali di base, necessari per l'attività motoria volontaria, mentre il sistema laterale si occupa, insieme alla via corticospinale diretta, dei movimenti delle estremità finalizzati ad uno scopo come raggiungere e manipolare oggetti.
- Gangli della base
I gangli della base sono strutture neuronali sottocorticali che sono coinvolte nell'elaborazione di informazioni motorie come la pianificazione e la programmazione di movimenti abili complessi e le cui alterazioni danno manifestazioni cliniche che sono raggruppate in sindromi note come "extrapiramidali".
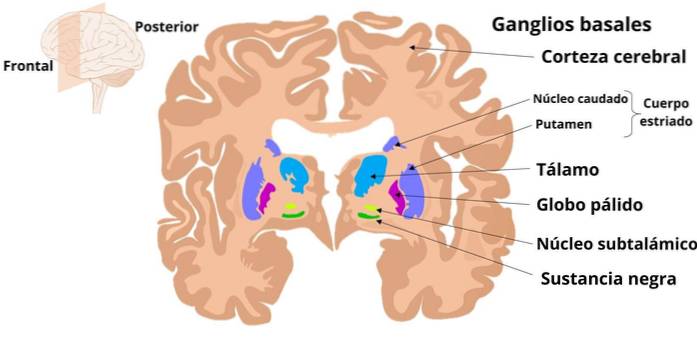
I gangli comprendono lo striato, che è costituito dal putamen e dal nucleo caudato; il globo pallido, che ha una porzione esterna (GPe) e una porzione interna (GPi); la substantia nigra, organizzata in una porzione compatta (SNc) e una porzione reticolata (SNr), e il nucleo subtalamico o di Lewis.
Queste strutture funzionano ricevendo informazioni principalmente da diverse regioni della corteccia cerebrale; informazioni che attivano circuiti interni che influenzano un'attività neuronale in uscita che ritorna, attraverso la porzione motoria del talamo, alla corteccia cerebrale.
- Connettività, percorso e neurochimica nei gangli della base
Le informazioni sui gangli entrano attraverso lo striato (caudato e putamen). Da lì partono percorsi che si collegano con i nuclei di uscita che sono GPi e SNr, i cui assoni vanno ai nuclei ventroanteriore e ventrolaterale del talamo, che, a loro volta, proiettano alla corteccia.
Le diverse fasi del circuito sono coperte da neuroni che appartengono a un particolare sistema neurochimico e che possono avere un effetto inibitorio o eccitatorio. Le connessioni cortico-striate, le fibre talamo-corticali e subtalamiche rilasciano glutammato e sono eccitatorie.
I neuroni i cui assoni escono dallo striato usano l'acido gamma ammino butirrico (GABA) come neurotrasmettitore principale e sono inibitori. Esistono due sottopopolazioni: una sintetizza la sostanza P come cotrasmettitore [GABA (+ Subst. P)] e l'altra encefalina [GABA (+ Encef.)].
Neuroni GABA (+ Subst. P)
I neuroni GABA (+ Sust. P) hanno recettori della dopamina D1 e sono eccitati dalla dopamina (DA); stabiliscono anche una connessione inibitoria diretta con gli sbocchi dei gangli della base (GPi e SNr) che sono anche GABAergici ma "+ dinorfina" e inibiscono le cellule glutamatergiche della proiezione talamo-corticale.
Neuroni GABA (+ Encepha.)
GABA (+ Encef.) I neuroni hanno recettori dopaminergici D2 e sono inibiti dalla dopamina. Stabiliscono una connessione eccitatoria indiretta con le uscite (GPi e SNr), poiché proiettano al GPe inibendo i suoi neuroni GABAergici, che inibiscono i neuroni glutamatergici del nucleo subtalamico, la cui funzione è quella di attivare le uscite (GPi e SNr).
La parte compatta della substantia nigra (SNc) ha neuroni dopaminergici (DA) che si connettono con lo striato realizzando connessioni, come già accennato, eccitatorie D1 sulle cellule GABA (+ Sub. P) e inibitorie D2 sulle cellule GABA (+ Encef.).
Quindi, e in accordo con quanto sopra, un'attivazione della via diretta finisce per inibire le uscite dei gangli della base e rilasciare l'attività nelle connessioni talamo-corticali, mentre l'attivazione della via indiretta attiva le uscite e riduce l'attività talamica. -corticale.
Sebbene le interazioni e l'esatto funzionamento articolare delle vie dirette e indirette appena considerate non siano state chiarite, l'organizzazione anatomica e neurochimica descritta ci aiuta a comprendere, almeno in parte, alcune condizioni patologiche derivanti dalla disfunzione dei gangli della base.
Malattie dei gangli della base
Sebbene i processi patologici che si insediano nei gangli della base siano di natura diversa e influenzino non solo alcune funzioni motorie ma anche cognitive, associative ed emotive, nei quadri clinici le alterazioni motorie occupano un posto di rilievo e la maggior parte della ricerca si è concentrata su di esse.
I disturbi del movimento tipici della disfunzione dei gangli della base possono essere classificati in uno di tre gruppi, vale a dire:
- Ipercinesia, come la malattia di Huntington o la corea e l'emibalismo.
- Ipocinesie, come il morbo di Parkinson.
- Distonie, come l'atetosi.
In termini generali si può affermare che i disturbi ipercinetici, caratterizzati da un'eccessiva attività motoria, si presentano con una diminuzione dell'inibizione che le uscite (GPi e SNr) esercitano sulle proiezioni talamo-corticali, che diventano più attive.
I disturbi ipocinetici, invece, sono accompagnati da un aumento di questa inibizione, con una riduzione dell'attività talamo-corticale.
malattia di Huntington
È un disturbo ipercinetico caratterizzato da scuotimento casuale involontario e spasmodico delle estremità e della regione orofacciale, movimenti coreiformi o "di danza" che aumentano gradualmente e inabilitano il paziente, disturbi del linguaggio e progressivo sviluppo della demenza.
La malattia è accompagnata precocemente da una degenerazione dei neuroni striatali GABA (+ Encef.) Della via indiretta.
Poiché questi neuroni non inibiscono più i neuroni GPe GABAergici, inibiscono eccessivamente il nucleo subtalamico, che cessa di eccitare le uscite inibitorie (GPi e SNr) e le proiezioni talamo-corticali vengono disinibite..
Emibalismo
Consiste nelle violente contrazioni dei muscoli prossimali degli arti, che vengono proiettati con forza in movimenti di grande ampiezza. Il danno in questo caso è la degenerazione del nucleo subtalamico, che si traduce in qualcosa di simile a quello descritto per la corea, sebbene non per iper inibizione, ma per distruzione del nucleo subtalamico.
morbo di Parkinson
È caratterizzato da difficoltà e ritardo nell'inizio dei movimenti (acinesia), rallentamento dei movimenti (ipocinesia), viso inespressivo o espressione facciale in una maschera, alterazione dell'andatura con diminuzione dei movimenti associati degli arti durante il movimento e tremore involontario dell'arto a riposo.
Il danno, in questo caso, consiste nella degenerazione del sistema nigrostriatale, che sono le proiezioni dopaminergiche che partono dalla regione compatta della substantia nigra (SNc) e si collegano con i neuroni striatali che danno origine alle vie dirette e indirette..
La soppressione dell'eccitazione che le fibre dopaminergiche esercitano sulle cellule GABA (+ Sust. P) della via diretta, rimuove l'inibizione che queste esercitano sugli sbocchi GABAergici (GPi e SNr) verso il talamo, che ora è più inibito. intensità. È quindi una disinibizione delle uscite.
D'altra parte, la soppressione dell'attività inibitoria che la dopamina esercita sulle cellule GABA (+ Encef.) Della via indiretta le rilascia e aumenta l'inibizione che esercitano sulle cellule GABA del GPe, che disinibisce i neuroni del nucleo subtalamico, che quindi iperattivano le uscite.
Come si può vedere, il risultato finale degli effetti della degenerazione dopaminergica sulle due vie interne, diretta e indiretta, è lo stesso, sia che si tratti di disinibizione o stimolazione delle uscite GABAergiche (GPi e SNr) che inibiscono i nuclei talamici e riducono la loro uscita nella corteccia, il che spiega l'ipocinesi
Riferimenti
- Ganong WF: Controllo riflesso e volontario di postura e movimento, in: Revisione di fisiologia medica, 25a ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Contributi del cervelletto e dei gangli basali al controllo motorio complessivo, in: Libro di testo di fisiologia medica, 13a edizione, AC Guyton, JE Hall (a cura di). Philadelphia, Elsevier Inc., 2016.
- Illert M: Motorisches System: Basalganglien, In: Physiologie, 4a ed; P Deetjen et al (eds). München, Elsevier GmbH, Urban & Fischer, 2005.
- Luhmann HJ: Sensomotorische systeme: Kórperhaltung und Bewegung, in: Fisiologia, 6a ed; R Klinke et al (eds). Stoccarda, Georg Thieme Verlag, 2010.
- Oertel WH: Basalganglienerkrankungen, in: Physiologie des Menschen mit Pathophysiologie, 31 ° ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Wichmann T e DeLong MR: The Basal Ganglia, In: Principles of Neural Science, 5a ed; E Kandel et al (eds). New York, McGraw-Hill, 2013.



Nessun utente ha ancora commentato questo articolo.