
Scoperta dei raggi anodici, proprietà

Il raggi anodici o raggi del canale, Chiamati anche positivi, sono fasci di raggi positivi costituiti da cationi atomici o molecolari (ioni caricati positivamente) che vengono diretti verso l'elettrodo negativo in un tubo di Crookes.
I raggi anodici si originano quando gli elettroni che vanno dal catodo verso l'anodo, entrano in collisione con gli atomi del gas racchiusi nel tubo di Crookes.

Quando particelle dello stesso segno si respingono, gli elettroni diretti verso l'anodo strappano gli elettroni presenti nella crosta degli atomi di gas..
Pertanto, gli atomi che sono rimasti caricati positivamente, cioè sono stati trasformati in ioni positivi (cationi), sono attratti dal catodo (caricati negativamente).
Indice articolo
- 1 Scoperta
- 2 Proprietà
- 3 Un po 'di storia
- 3.1 Il tubo a raggi anodici
- 3.2 Il protone
- 3.3 Spettrometria di massa
- 4 Riferimenti
Scoperta
Fu il fisico tedesco Eugen Goldstein a scoprirli, osservandoli per la prima volta nel 1886.
Successivamente, il lavoro svolto sui raggi anodici dagli scienziati Wilhelm Wien e Joseph John Thomson finì per ipotizzare lo sviluppo della spettrometria di massa.
Proprietà
Le principali proprietà dei raggi anodici sono le seguenti:
- Hanno una carica positiva, il cui valore è un multiplo intero della carica dell'elettrone (1,6 ∙ 10-19 C).
- Si muovono in linea retta in assenza di campi elettrici e magnetici.
- Deviano in presenza di campi elettrici e magnetici, spostandosi verso la zona negativa.
- Può penetrare in strati sottili di metalli.
- Possono ionizzare i gas.
- Sia la massa che la carica delle particelle che compongono i raggi anodici variano a seconda del gas racchiuso nel tubo. Normalmente la loro massa è identica alla massa degli atomi o delle molecole da cui derivano..
- Possono causare cambiamenti fisici e chimici.
Un po 'di storia
Prima della scoperta dei raggi anodici, avvenne la scoperta dei raggi catodici, avvenuta negli anni 1858 e 1859. La scoperta si deve a Julius Plücker, matematico e fisico di origine tedesca..
Successivamente, fu il fisico inglese Joseph John Thomson a studiare in profondità il comportamento, le caratteristiche e gli effetti dei raggi catodici.
Da parte sua, Eugen Goldstein - che in precedenza aveva svolto altre indagini con i raggi catodici - fu colui che scoprì i raggi anodici. La scoperta avvenne nel 1886 e lo fece quando si rese conto che i tubi a scarica con il catodo perforato emettevano luce anche all'estremità del catodo.
In questo modo scoprì che, oltre ai raggi catodici, c'erano altri raggi: raggi anodici; questi si stavano muovendo nella direzione opposta. Poiché questi raggi passavano attraverso i fori o canali nel catodo, decise di chiamarli raggi di canale..
Tuttavia, non fu lui, ma Wilhelm Wien, che in seguito fece ampi studi sui raggi anodici. Wien, insieme a Joseph John Thomson, finì per stabilire le basi per la spettrometria di massa.
La scoperta di Eugen Goldstein sui raggi anodici costituì un pilastro fondamentale per lo sviluppo successivo della fisica contemporanea..
Grazie alla scoperta dei raggi anodici si sono resi disponibili per la prima volta sciami di atomi in rapido e ordinato movimento, la cui applicazione è stata molto fertile per diversi rami della fisica atomica..
Il tubo a raggi anodici
Nella scoperta dei raggi anodici, Goldstein ha utilizzato un tubo di scarica che aveva il catodo perforato. Il processo dettagliato mediante il quale si formano i raggi anodici in un tubo a scarica di gas è il seguente.
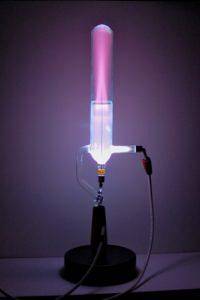
Applicando una grande differenza di potenziale di diverse migliaia di volt al tubo, il campo elettrico che si crea accelera il piccolo numero di ioni che sono sempre presenti in un gas e che vengono creati da processi naturali come la radioattività..
Questi ioni accelerati entrano in collisione con gli atomi del gas, strappando loro elettroni e creando ioni più positivi. A loro volta, questi ioni ed elettroni attaccano di nuovo più atomi, creando più ioni positivi in quella che è una reazione a catena..
Gli ioni positivi sono attratti dal catodo negativo e alcuni passano attraverso i fori nel catodo. Quando raggiungono il catodo, hanno già accelerato abbastanza velocemente che quando entrano in collisione con altri atomi e molecole nel gas, eccitano la specie a livelli di energia più elevati..
Quando queste specie ritornano ai loro livelli energetici originali, gli atomi e le molecole rilasciano l'energia che avevano acquisito in precedenza; l'energia viene emessa sotto forma di luce.
Questo processo di produzione della luce, chiamato fluorescenza, fa apparire un bagliore nella regione in cui gli ioni emergono dal catodo.
Il protone
Sebbene Goldstein abbia ottenuto i protoni con i suoi esperimenti con i raggi anodici, la verità è che non è lui a essere accreditato della scoperta del protone, poiché non è stato in grado di identificarlo correttamente.
Il protone è la più leggera delle particelle positive prodotte nei tubi a raggi anodici. Il protone viene prodotto quando il tubo viene caricato con idrogeno gassoso. In questo modo, quando l'idrogeno ionizza e perde il suo elettrone, si ottengono protoni..
Il protone ha una massa di 1,67 ∙ 10-24 g, quasi uguale a quella dell'atomo di idrogeno, e ha la stessa carica ma di segno opposto a quella dell'elettrone; cioè 1,6 ∙ 10-19 C.
Spettrometria di massa
La spettrometria di massa, sviluppata dalla scoperta dei raggi anodici, è una procedura analitica che permette di studiare la composizione chimica delle molecole di una sostanza in base alla loro massa..
Permette sia di riconoscere composti sconosciuti, di contare composti noti, sia di conoscere le proprietà e la struttura delle molecole di una sostanza.
Da parte sua, lo spettrometro di massa è un dispositivo con cui è possibile analizzare in modo molto preciso la struttura di diversi composti chimici e isotopi..
Lo spettrometro di massa consente la separazione dei nuclei atomici in base alla relazione tra massa e carica.

Riferimenti
-
- Raggio anodico (n.d.). Su Wikipedia. Estratto il 19 aprile 2018 da es.wikipedia.org.
- Raggio anodico (n.d.). Su Wikipedia. Estratto il 19 aprile 2018 da en.wikipedia.org.
- Spettrometro di massa (n.d.). Su Wikipedia. Estratto il 19 aprile 2018 da es.wikipedia.org.
- Grayson, Michael A. (2002). Misurazione della massa: dai raggi positivi alle proteine. Philadelphia: Chemical Heritage Press
- Grayson, Michael A. (2002). Misurazione della massa: dai raggi positivi alle proteine. Philadelphia: Chemical Heritage Press.
- Thomson, J. J. (1921). Raggi di elettricità positiva e loro applicazione alle analisi chimiche (1921)
- Fidalgo Sánchez, José Antonio (2005). Fisica e chimica. Everest



Nessun utente ha ancora commentato questo articolo.