
Quali basi chimiche si possono trovare in casa?
Il basi chimiche Sono presenti in un gran numero di prodotti per l'uso quotidiano a casa e in alcuni alimenti che potresti nemmeno immaginare. Dopotutto, la scienza è ovunque.
Quando stavo iniziando i miei studi di chimica all'università, uno dei miei professori ci esortava ad essere curiosi e investigativi, qualità che caratterizzano un bravo scienziato..

Ispirato dalle sue parole, ho preso un rotolo di cartina di tornasole e ho iniziato a misurare il pH di tutto quello che avevo in casa. La verità è che sono rimasto molto sorpreso dalla quantità di cose che avevano un pH di base in casa.
In effetti, ricordo che l'unica cosa che ha cambiato la cartina al tornasole in rossa è stata la salsa di pomodoro ketchup (il che ha senso dato che i suoi ingredienti sono pomodoro e aceto).
Come ho già detto in altri articoli, una base è un composto chimico con la capacità di accettare protoni, donare idrossile o possedere una coppia di elettroni liberi. Hanno la proprietà di neutralizzare gli acidi, aumentare il pH di una soluzione e rendere blu la cartina di tornasole..
Le basi sono molto importanti nell'uso quotidiano e spesso passano inosservate. Senza basi, le macchie persistenti sui vestiti non si staccerebbero, si avrebbero specchi sporchi e persino problemi intestinali come reflusso gastrico e costipazione non potrebbero essere alleviati (SPM Chemistry Form 4 Notes - Acids and Bases (Part 2), 2013).
Di seguito fornisco un elenco di basi di utilizzo quotidiano che, all'epoca, davano una colorazione bluastra alla cartina di tornasole. Tutte queste basi sono nei prodotti di uso quotidiano e alimentare (Acids vs. Bases, S.F.).
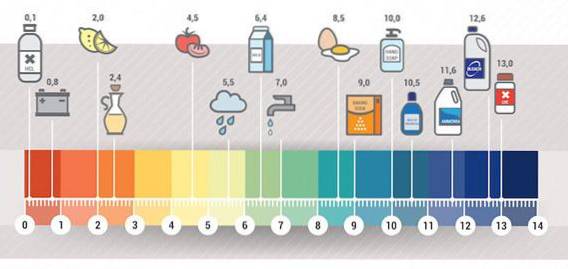
Esempi di basi che troviamo in casa
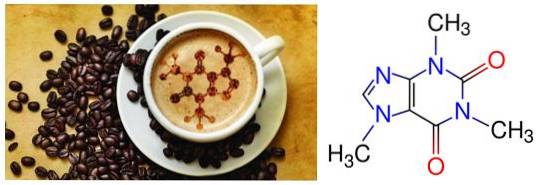
1- Caffè e tè: la molecola della caffeina (1,3,7 trimetilxantina) prende il nome da essa perché è stata scoperta nei chicchi di caffè.
Successivamente si è scoperto che esiste anche nelle foglie di tè in maggiore concentrazione. Questa molecola, una purina molto simile all'adenina e, come essa, è una base azotata.
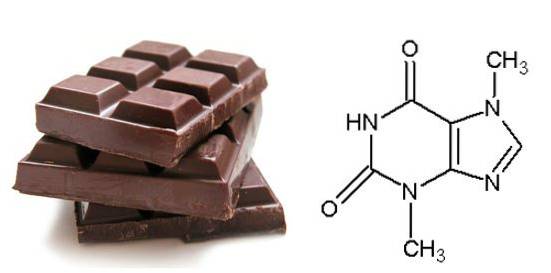
2- CioccolatoSimile al caffè, il cioccolato contiene un composto chiamato teobromina che è una base di azoto purinico.
Questo composto è responsabile del gusto del cioccolato così buono, tuttavia, cani e gatti non metabolizzano la teobromina, che causa danni al cuore e al sistema nervoso centrale. In conclusione, non dare mai cioccolato al tuo animale domestico (Reactions, 2016).
3- Cloro: il cloro è in realtà ipoclorito o clorito di sodio, a seconda che si tratti di cloro da piscine o cloro per lavare i panni.
Gli ioni ipoclorito e clorito sono le basi coniugate degli acidi ipocloroso e cloruro rispettivamente che in soluzione acquosa hanno la capacità di prelevare protoni dall'acqua, aumentando la concentrazione di idrossile nel mezzo (Acidi e Basi - Applicazioni nella vita reale, S.F.).
ClO- + HDueO → HClO + OH-
ClODue- + HDueO → HClODue + Oh-
4- candeggina: La base più resistente disponibile in commercio, pulisce i forni e sblocca i tubi. La candeggina, o idrossido di sodio (NaOH), è un componente principale nei detergenti per scarichi, liquefacendo i rifiuti in modo che possano essere lavati attraverso i tubi.
I detergenti per forno a base di candeggina caustica tagliano il materiale cotto nel forno. Deve essere maneggiato con cura poiché può causare gravi ustioni chimiche.

Il bicarbonato di sodio è sicuro da toccare. Bere qualche pizzico di bicarbonato di sodio sciolto in acqua neutralizzerà parte dell'acido in eccesso nello stomaco. Inoltre, è un detergente leggermente abrasivo e non tossico.
6- Borace: noto anche come tetraborato di sodio (NaDueB4O7 ● 10HDueO) una volta ha contribuito a preservare le mummie nell'antico Egitto. Ora mantiene i vestiti freschi e uccide i parassiti in casa. Il suo pH di 9,2 significa che è 920 volte più alcalino dell'acqua pura.
Il borace fornisce all'acqua uno ione ossigeno per formare il perossido di idrogeno (H.DueODue) in soluzione, rendendolo un disinfettante e un blando agente sbiancante.
Evita di maneggiare il borace direttamente o troppo a lungo in quanto può causare irritazione alla pelle. Il borace è leggermente tossico se ingerito. (Whitney, 2017).
7- Ammoniaca: il termine "ammoniaca" si riferisce sia ad un gas irritante (NH3) e il prodotto per la pulizia (NH4OH) che risulta dalla dissoluzione dell'ammoniaca in acqua. L'ammoniaca domestica ha un pH di 11, o 50 volte più forte di quello del latte di magnesia.
È un potente detergente domestico che pulisce praticamente qualsiasi superficie da sporco e grasso (Cascio, 2017).

9- Latte di magnesia: Questo comune antiacido e lassativo ha preso il nome lattiginoso per la sua opacità. Idrossido di magnesio [Mg (OH)Due] ha un pH di 10,5. I preparati commerciali a base di latte di magnesia utilizzano aromi di menta o frutta per nascondere il sapore amaro caratteristico delle sostanze alcaline..
10- Antiacidi: L'uso di basi deboli per alleviare il bruciore di stomaco è comune. Composti come il bicarbonato di sodio (NaHCO3), carbonato di magnesio (MgCO3), carbonato di calcio (CaCO3) e idrossido di alluminio (Al (OH)3) sono i principi attivi degli antiacidi.
11- Deodoranti- L'idrossido di alluminio è anche il principio attivo dei deodoranti. Agisce come battericida, eliminando i batteri che si nutrono delle proteine e dei grassi nel sudore secreti dalle ghiandole apocrine (Reaction, 2015).
12- Sapone: il sapone è il prodotto della neutralizzazione dell'idrossido di sodio e dell'acido stearico. Quest'ultimo è un acido grasso saturo con 18 atomi di carbonio.

Il prodotto di questa neutralizzazione è lo stearato di sodio, che in soluzione acquosa forma lo ione stearato.
Questa molecola contiene una parte polare e una non polare, motivo per cui è nota come molecola anfipatica e sono responsabili della rimozione di grassi e altri composti alifatici dai vestiti o dal corpo.
Riferimenti
- Acidi e basi - Applicazioni nella vita reale. (S.F.). Recupero da scienceclarified.com.
- Acidi vs. Basi. (S.F.). Recupero da acid-vs-bases.weebly.com.
- Cascio, C. (2017, 25 aprile). Esempi di acidi e basi del mondo reale. Recuperato da sciencing.com.
- (2015, 21 settembre). Come funzionano i deodoranti e gli antitraspiranti? . Recuperato da youtube.com.
- Reazioni. (2016, 18 gennaio). Perché il cioccolato fa male ai cani? . Recuperato da youtube.com.
- SPM Chemistry Form 4 Notes - Acids and Bases (Part 2). (2013, 2 marzo). Recupero da berryberryeasy.com.
- Whitney, L. (2017, 25 aprile). Basi utilizzate come prodotti domestici comuni. Recuperato da sciencing.com.

Nessun utente ha ancora commentato questo articolo.