
Caratteristiche, struttura, tipi, funzioni della lipasi
Il lipasi costituiscono una grande famiglia di enzimi in grado di catalizzare l'idrolisi dei legami esterei presenti in substrati quali trigliceridi, fosfolipidi, esteri del colesterolo e alcune vitamine.
Sono presenti praticamente in tutti i regni della vita, sia in microrganismi come batteri e lieviti, sia in piante e animali; in ogni tipo di organismo questi enzimi hanno proprietà e caratteristiche speciali che li differenziano l'uno dall'altro.
A seconda del tipo di classificazione, è possibile distinguere tra lipasi "vere", note anche come lipasi triacilgliceroliche, e altri enzimi con attività lipolitica simile come fosfolipasi, steroli esterasi e retinil palmitato esterasi..
Il primo rapporto pubblicato sulla sequenza di un enzima lipasi fu quello di De Caro et al.Nel 1981, che studiava la triacilglicerolo lipasi pancreatica dei suini. Studi successivi hanno dimostrato l'esistenza di molte altre lipasi sistemiche negli organismi viventi..
Le lipasi più importanti negli animali sono le lipasi digestive prodotte dal pancreas e dal fegato, che partecipano al metabolismo dei grassi consumati regolarmente nella dieta, e quindi hanno importanti risvolti fisiologici da vari punti di vista.
Attualmente questi enzimi non sono solo studiati per scopi clinici e / o metabolici, ma sono anche prodotti industrialmente per scopi commerciali per la lavorazione di alimenti e altri prodotti, e possono essere ottenuti dalla coltivazione di speciali microrganismi..
Indice articolo
- 1 Caratteristiche
- 1.1 Meccanismo catalitico
- 1.2 Specificità del substrato
- 2 Struttura
- 2.1 Lipasi pancreatica umana
- 3 funzioni
- 3.1 Funzioni industriali
- 4 Riferimenti
Caratteristiche
Le lipasi sono proteine idrosolubili e catalizzano reazioni idrolitiche su substrati insolubili. Si trovano in natura in un equilibrio tra le loro forme attive e inattive e l'attivazione o l'inattivazione dipende da diversi fattori cellulari interni..
Appartengono alla superfamiglia degli enzimi idrolasi con pieghe α / β, dove sono classificate anche esterasi, tioesterasi, alcune proteasi e perossidasi, dalogenasi e altre idrolasi intracellulari..
Le lipasi sono codificate da geni che appartengono a una famiglia che include geni che codificano per lipasi pancreatica, lipasi epatica, lipoproteina lipasi, lipasi endoteliale e fosfatidilserina fosfolipasi A1..
Meccanismo catalitico
Alcuni autori propongono che la forma di catalisi che hanno questi enzimi sia analoga a quella delle serina proteasi, che è correlata alla presenza di tre speciali residui amminoacidici nel sito attivo.
Il meccanismo di idrolisi prevede la formazione di un complesso enzima-substrato (lipasi: trigliceride), successivamente la formazione di un intermedio emiacetale e quindi il rilascio di un diacilgliceride e di un acido grasso..
L'ultimo passaggio dell'idrolisi, il rilascio dell'acido grasso dal sito attivo, avviene secondo un modello noto come modello "catapulta", il che implica che dopo la scissione o la rottura del legame estereo, l'acido grasso viene rapidamente espulso dal sito catalitico.
Specificità del substrato
Le lipasi possono essere specifiche e differenziare tra substrati come trigliceridi, diacilgliceridi, monogliceridi e fosfolipidi. Alcuni sono specifici in termini di acidi grassi, cioè per quanto riguarda la loro lunghezza, il loro grado di saturazione, ecc..
Possono anche essere selettivi in termini di regione in cui catalizzano l'idrolisi, ciò significa che possono avere specificità di posizione rispetto al sito a cui le molecole di acido grasso si legano alla spina dorsale del glicerolo (in uno qualsiasi dei tre atomi di carbonio)..
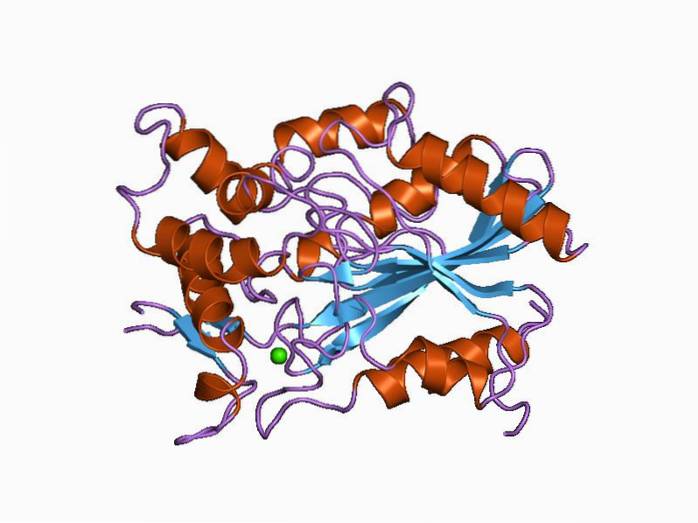
Struttura
Come gli altri membri della famiglia enzimatica a cui appartengono, le lipasi sono caratterizzate da una topologia composta da α-eliche e fogli β-piegati. Il sito catalitico di questi enzimi è generalmente composto da una triade di amminoacidi: serina, acido aspartico o glutammico e istidina..
La maggior parte delle lipasi sono glicoproteine che, a seconda delle dimensioni della porzione di carboidrati, hanno un peso molecolare compreso tra 50 e 70 kDa..
Lipasi pancreatica umana
Ha 449 residui amminoacidici e due domini separati: uno N-terminale, dove si trovano il sito catalitico e la caratteristica piega delle idrolasi (α / β), e un altro C-terminale, di dimensioni più piccole e considerato "ausiliario", con una struttura chiamata "β-sandwich".
Il suo peso molecolare è compreso tra 45 e 53 kDa e la sua attività catalitica è maggiore a temperature prossime a 37 ° C e a pH compreso tra 6 e 10.
Caratteristiche
A seconda dell'organo in cui si trovano nei mammiferi, ad esempio, le lipasi esercitano funzioni fisiologiche alquanto diverse.
Come accennato, sono presenti lipasi specifiche nel pancreas, nel fegato, nelle ovaie e nelle ghiandole surrenali (nei reni) e nei tessuti endoteliali..
Le lipasi epatiche sono responsabili del metabolismo delle particelle di lipoproteine, che sono complessi formati da lipidi e proteine che funzionano principalmente nel trasporto di trigliceridi e colesterolo tra organi e tessuti..
In particolare, le lipasi partecipano all'idrolisi o al rilascio di acidi grassi dalle molecole di trigliceridi contenute nelle lipoproteine. Ciò è necessario per estrarre energia da queste molecole o per riciclarle, utilizzandole come precursori nella sintesi di altri composti..
Le lipasi endoteliali sono presenti nel fegato, nei polmoni, nella tiroide e negli organi riproduttivi e l'espressione dei loro geni è regolata da diverse citochine. Questi enzimi sono anche coinvolti nel metabolismo delle lipoproteine..
Funzioni industriali
Nell'industria lattiero-casearia è comune l'uso delle lipasi per idrolizzare i grassi presenti nel latte, che ha effetti diretti sul "potenziamento" del sapore di formaggi, creme e altri prodotti lattiero-caseari..
Sono utilizzati anche nella fabbricazione di altri prodotti alimentari, soprattutto durante la fermentazione, al fine di migliorare il gusto e la "digeribilità" di alcuni cibi preparati industrialmente..
Lontano dall'industria alimentare, l'uso di lipasi di origine microbica è diffuso nella formulazione di detergenti e sostanze per la pulizia generale, che riducono gli effetti nocivi sull'ambiente causati dall'enorme carico chimico presente nei prodotti di pulizia convenzionali..
Riferimenti
- Lowe, M. E. (2002). Le lipasi trigliceridiche del pancreas. Giornale di ricerca sui lipidi, 43, 2007-2016.
- Mead, J. R., Irvine, S. A., e Ramji, D. P. (2002). Lipoproteina lipasi: struttura, funzione, regolazione e ruolo nella malattia. J. Mol. Med., 80, 753-769.
- Perret, B., Mabile, L., Martinez, L., Tercé, F., Barbaras, R. e Collet, X. (2002). Lipasi epatica: relazione struttura / funzione, sintesi e regolazione. Giornale di ricerca sui lipidi, 43, 1163-1169.
- Santamarina-fojo, S., González-navarro, H., Freeman, L., Wagner, E., Santamarina-fojo, S., Gonza, H.,… Nong, Z. (2004). Lipasi epatica, metabolismo delle lipoproteine e aterogenesi. Arteriosclerosi, trombosi e biologia vascolare, 24, 1750-1754.
- Taylor, P., Kurtovic, I., Marshall, S. N., Zhao, X., Simpson, B. K., Kurtovic, I.,… Zhao, X. I. N. (2012). Lipasi di mammiferi e pesci. Recensioni in Fisheries Science, 29, 37-41.


Nessun utente ha ancora commentato questo articolo.