
Gilbert Newton Lewis Biografia e contributi alla scienza
Gilbert Newton Lewis È stato uno dei più importanti scienziati americani del XX secolo. Il suo lavoro ha prodotto una rivoluzione strutturale negli studi chimici, grazie ai numerosi contributi che ha dato nel corso della sua vita allo sviluppo della scienza..
Tra i contributi di questo fisico-chimico spicca la formula che porta il suo nome, con la quale vengono rappresentate graficamente le sole coppie di elettroni. Il lavoro di ricerca di Lewis fu molto ampio, sebbene la sua fama fosse fondamentalmente dovuta alla teoria sui legami chimici e alla definizione di acido-base formulata nel 1923.

Lewis ha avuto una grande influenza nel mondo scientifico e accademico degli Stati Uniti, in particolare all'Università di Harvard, dove si è formato e ha insegnato. Il suo lavoro per l'esercito degli Stati Uniti durante la prima guerra mondiale gli valse il massimo riconoscimento e le più alte onorificenze..
Si è formato nelle università del Nebraska, Harvard, Lipsia e Gottinga in Germania. Ha lavorato presso il Massachusetts Institute of Technology (MIT), l'Università di Harvard e l'Università della California, dove è morto lavorando.
Nel corso della sua vita ha ricevuto innumerevoli riconoscimenti e premi, tra cui diversi dottorati honoris causa dalle università di Chicago, Madrid, Liverpool, Wisconsin e Pennsylvania. È stato membro onorario di varie istituzioni scientifiche in Inghilterra, India, Svezia, Danimarca e Stati Uniti..
Indice articolo
- 1 Biografia
- 1.1 Studi
- 1.2 Lavoro accademico e partecipazione alla guerra
- 1.3 Morte in laboratorio
- 2 Contributi alla scienza
- 2.1 Strutture di Lewis
- 2.2 Legame covalente
- 2.3 Teoria dell'ottetto
- 2.4 Photon
- 2.5 Attrazione chimica e valenza
- 2.6 Acqua pesante
- 2.7 Teoria delle soluzioni
- 3 Riferimenti
Biografia
Gilbert Newton Lewis nacque a Weymouth, Massachusetts, il 23 ottobre 1875. I suoi genitori erano Frank Wesley Lewis e Mary Burr White Lewis. Durante i suoi primi anni fu insegnato a casa sua e all'età di 10 anni entrò nella scuola pubblica, diplomandosi nel 1889.
Nel 1884 Lewis dovette stabilirsi con la sua famiglia a Lincoln, nel Nebraska. All'età di 13 anni, è stato ammesso alla University of Nebraska High School..
Studi
Dopo la laurea, ha proseguito i suoi studi universitari per due anni e poi si è iscritto all'Università di Harvard nel 1893.
Inizialmente era interessato all'economia, ma alla fine ha optato per la fisica e la chimica. Gilbert si laureò in chimica nel 1896 e per un anno insegnò alla Phillips Academy, una scuola privata di Andover..
Tornò ad Harvard per un lavoro post-laurea e un master nel 1898 con la sua tesi su L'elettrone e una molecola. Un anno dopo ha conseguito il dottorato e la sua tesi è stata intitolata Alcune relazioni elettrochimiche e termochimiche di amalgami di zinco e cadmio".
Ad Harvard ha servito come istruttore per un anno, poi ha viaggiato in Europa con una borsa di studio. Ha studiato con i grandi fisico-chimici del tempo.
Nel 1899 si recò in Germania per studiare con Wilhelm Ostwald Leipzig e successivamente con Walter Nernst all'Università di Gottinga; poi ha lavorato per il governo filippino.
Lavoro accademico e partecipazione alla guerra
Tra il 1999 e il 1906 ha insegnato chimica all'Università di Harvard e in seguito è stato assunto dal Massachusetts Institute of Technology, dove è stato dal 1907 al 1912.
In seguito divenne professore di chimica fisica presso l'Università della California (Berkeley), dove ottenne il grado di preside della School of Chemistry..
Nel 1908 pubblicò il suo primo articolo sulla teoria della relatività in parallelo con Albert Einstein. In questo stabilisce che esiste un legame tra energia-massa, ma in una direzione diversa da quella usata da Einstein..
Il 21 giugno 1912 Lewis sposò Mary Hinckley Sheldon, dalla quale ebbe tre figli: Margery S. Lewis, Edward S. Lewis e Richard Newton Lewis..
Il suo lavoro in California fu interrotto dallo scoppio della prima guerra mondiale. Nel 1917 fu incaricato di lavorare per l'esercito degli Stati Uniti, dove divenne capo della divisione di difesa del servizio di guerra chimica..
La dedizione e la capacità di lavorare di Lewis permise all'esercito di ridurre il numero di vittime che aveva subito fino a quel momento a causa dell'uso del gas da parte degli eserciti nemici. Alla fine della guerra, è stato insignito delle più alte onorificenze per i suoi servizi.
Morte in laboratorio
Gilbert N. Lewis morì all'età di 70 anni per un attacco di cuore mentre lavorava nel suo laboratorio presso l'Università di Berkeley, il 23 marzo 1946..
Forse a causa della sua personalità introversa, questo eminente scienziato non ha mai ricevuto il premio Nobel. Quasi alla fine della sua carriera è riuscito a dimostrare che la fosforescenza delle molecole organiche è governata da uno stato di tripletto eccitato, arrivando addirittura a calcolarne le proprietà magnetiche..
Contributi alla scienza
Alcuni dei contributi più importanti di Gilbert Newton Lewis alla scienza sono i seguenti:
Strutture di Lewis
Esistono diversi metodi che servono a rappresentare la struttura di una molecola. In questi i simboli degli elementi rappresentano gli atomi, mentre i punti rappresentano gli elettroni che li circondano. Un esempio di ciò è la rappresentazione di idrogeno, elio e carbonio:
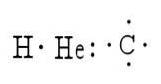
Lewis fu il primo a proporre l'idea che gli atomi potessero stare insieme confrontando coppie di elettroni; ecco perché ha creato il simbolismo delle strutture.
La teoria dell'ampio legame proposta da Lewis servì a raggruppare in un unico concetto tutti i tipi di legami chimici. In questo modo è stato possibile dimostrare le relazioni tra sostanze ioniche, molecolari, covalenti e metalliche. Fino a quel momento, questi elementi non avevano avuto alcuna connessione concettuale..
Legame covalente
Ha concettualizzato il legame covalente che si forma tra due atomi quando si uniscono per ottenere l'ottetto stabile e condividere gli elettroni dell'ultimo livello, ad eccezione dell'idrogeno, che riesce a raggiungere la stabilità avendo 2 elettroni.
Teoria dell'ottetto
Fu enunciato da Lewis nel 1916. In questo si stabilisce che gli ioni appartenenti agli elementi del sistema periodico tendono a completare i loro ultimi livelli di energia con un numero di 8 elettroni. Ciò consente loro di acquisire una configurazione molto stabile.
Fotone
Fu il creatore nel 1926 del termine fotone per designare la più piccola unità di energia luminosa. Questa particella di energia trasmette tutte le forme esistenti di radiazione elettromagnetica (raggi X, infrarossi, gamma, ultravioletti, microonde, onde radio, ecc.).
Attrazione chimica e valenza
Insieme al suo collega chimico Irwing Langmuir, ha sviluppato la teoria dell'attrazione chimica e della valenza, nota come teoria di Langmuir-Lewis. Per questo ha fatto affidamento sulla struttura atomica delle sostanze.
Acqua pesante
Lewis è stato anche il primo scienziato a studiare e produrre acqua pesante (deuterio) allo stato puro. Fu anche il primo ad applicare i principi della termodinamica nello studio dei problemi chimici..
Teoria della soluzione
Allo stesso modo, Lewis è riconosciuto per il suo lavoro sulla teoria delle soluzioni; ovvero le miscele omogenee che si ottengono dall'interposizione di atomi, molecole o ioni presenti in due o più sostanze. Queste sostanze chiamate componenti sono coinvolte in proporzioni variabili.
Riferimenti
- Gilbert Newton Lewis (1875-1946). Accademia nazionale delle scienze (PDF). Consultato su nasonline.org.
- Figure storiche in chimica: Gilbert Newton Lewis (1875-1946). Consultato da uv.es
- Gilbert Newton Lewis. Consultato su historia-biografia.com
- Gilbert Newton Lewis. Consultato su biografiasyvidas.com
- Biografia di Gilbert N. Lewis. Consultato su biographies.wiki
- 7 cose che devi davvero sapere su Gilbert Newton Lewis, lo scienziato che ha quasi battuto Einstein. Consultato su vix.com
- Gilbert Lewis e il centenario della teoria del legame di coppia di elettroni (Parte 1). Consultato su bicsociety.org



Nessun utente ha ancora commentato questo articolo.