
Stadi, funzioni e inibitori della fosforilazione ossidativa
Il fosforilazione ossidativa è un processo in cui le molecole di ATP vengono sintetizzate da ADP e Pio (fosfato inorganico). Questo meccanismo è svolto da batteri e cellule eucariotiche. Nelle cellule eucariotiche, la fosforilazione avviene nella matrice mitocondriale delle cellule non fotosintetiche.
La produzione di ATP è guidata dal trasferimento di elettroni dai coenzimi NADH o FADHDue alla ODue. Questo processo rappresenta la più alta produzione di energia nella cellula ed è derivato dalla scomposizione di carboidrati e grassi..
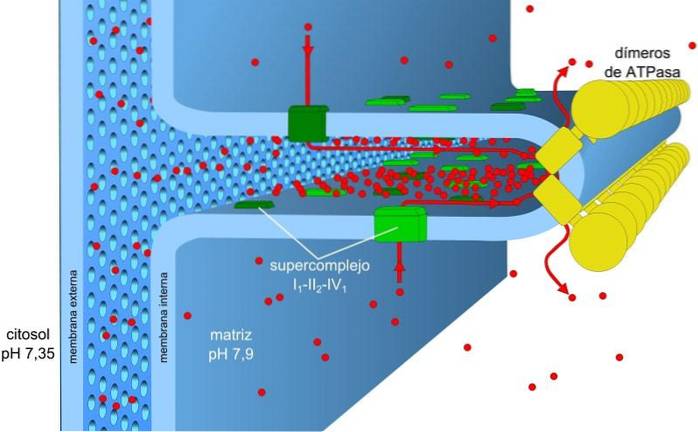
L'energia immagazzinata nella carica e nei gradienti di pH, nota anche come forza motrice del protone, consente che questo processo abbia luogo. Il gradiente protonico che si genera fa sì che la parte esterna della membrana abbia una carica positiva a causa della concentrazione di protoni (H+) e la matrice mitocondriale è negativa.
Indice articolo
- 1 Dove si verifica la fosforilazione ossidativa?
- 1.1 Centrale elettrica cellulare
- 2 fasi
- 2.1 Catena di trasporto degli elettroni
- 2.2 Succinato CoQ reduttasi
- 2.3 Accoppiamento o trasduzione di energia
- 2.4 Accoppiamento chemosmotico
- 2.5 sintesi di ATP
- 3 prodotti
- 4 funzioni
- 5 Controllo della fosforilazione ossidativa
- 5.1 Controllo coordinato della produzione di ATP
- 5.2 Controllo da parte dell'accettatore
- 5.3 Agenti di disaccoppiamento
- 5.4 Inibitori
- 6 Riferimenti
Dove si verifica la fosforilazione ossidativa?
I processi di trasporto degli elettroni e fosforilazione ossidativa sono associati a una membrana. Nei procarioti questi meccanismi vengono eseguiti attraverso la membrana plasmatica. Nelle cellule eucariotiche si associano alla membrana mitocondriale.
Il numero di mitocondri trovati nelle cellule varia a seconda del tipo di cellula. Ad esempio, nei mammiferi, gli eritrociti mancano di questi organelli, mentre altri tipi di cellule, come le cellule muscolari, possono averne fino a milioni..
La membrana mitocondriale è costituita da una semplice membrana esterna, una membrana interna un po 'più complessa e tra di esse lo spazio intermembrana, dove si trovano molti enzimi dipendenti dall'ATP.
La membrana esterna contiene una proteina chiamata porina che forma i canali per la semplice diffusione di piccole molecole. Questa membrana è responsabile del mantenimento della struttura e della forma dei mitocondri.
La membrana interna ha una densità maggiore ed è ricca di proteine. Inoltre è impermeabile alle molecole e agli ioni quindi, per attraversarlo, hanno bisogno di proteine intermembrane per trasportarli..
All'interno della matrice, le pieghe della membrana interna si estendono, formando creste che le consentono di avere una vasta area in un piccolo volume.
Centrale elettrica delle cellule
Il mitocondrio è considerato il produttore centrale di energia cellulare. Contiene gli enzimi coinvolti nei processi del ciclo dell'acido citrico, l'ossidazione degli acidi grassi e gli enzimi redox e le proteine per il trasporto degli elettroni e la fosforilazione dell'ADP.
Il gradiente di concentrazione del protone (gradiente di pH) e il gradiente di carica o potenziale elettrico nella membrana interna dei mitocondri sono responsabili della forza motrice del protone. La bassa permeabilità della membrana interna per gli ioni (diversi da H.+) consente ai mitocondri di avere un gradiente di tensione stabile.
Il trasporto elettronico, il pompaggio di protoni e l'ottenimento di ATP avvengono simultaneamente nei mitocondri, grazie alla forza motrice del protone. Il gradiente di pH mantiene condizioni acide nell'intermembrana e nella matrice mitocondriale con condizioni alcaline.
Per ogni due elettroni trasferiti a ODue circa 10 protoni vengono pompati attraverso la membrana, creando un gradiente elettrochimico. L'energia rilasciata in questo processo viene prodotta gradualmente dal passaggio di elettroni attraverso la catena di trasporto.
Fasi
L'energia rilasciata durante le reazioni di riduzione dell'ossidazione di NADH e FADHDue è notevolmente alto (circa 53 kcal / mol per ogni coppia di elettroni), quindi per essere utilizzato nella fabbricazione di molecole di ATP, deve essere prodotto gradualmente con il passaggio degli elettroni attraverso trasportatori.
Questi sono organizzati in quattro complessi situati sulla membrana mitocondriale interna. L'accoppiamento di queste reazioni alla sintesi di ATP viene effettuato in un quinto complesso.
Catena di trasporto degli elettroni
NADH trasferisce una coppia di elettroni che entrano nel complesso I della catena di trasporto degli elettroni. Gli elettroni vengono trasferiti al flavina mononucleotide e quindi all'ubiquinone (coenzima Q) attraverso un trasportatore ferro-zolfo. Questo processo rilascia una grande quantità di energia (16,6 kcal / mol).
L'ubiquinone trasporta gli elettroni attraverso la membrana al complesso III. In questo complesso gli elettroni passano attraverso i citocromi bec1 grazie a un trasportatore ferro-zolfo.
Gli elettroni passano dal complesso III al complesso IV (citocromo c ossidasi), trasferiti uno ad uno nel citocromo c (proteina della membrana periferica). Nel complesso IV gli elettroni passano attraverso una coppia di ioni rame (CuperDue+), seguito dal citocromo cper, poi ad un'altra coppia di ioni rame (CubDue+) e da questo al citocromo a3.
Infine, gli elettroni vengono trasferiti a ODue che è l'ultimo accettore e forma una molecola d'acqua (H.DueO) per ogni coppia di elettroni ricevuti. Il passaggio di elettroni dal complesso IV a ODue Genera anche una grande quantità di energia libera (25,8 kcal / mol).
Succinato CoQ reduttasi
Il complesso II (succinato CoQ reduttasi) riceve una coppia di elettroni dal ciclo dell'acido citrico, mediante l'ossidazione di una molecola di succinato in fumarato. Questi elettroni vengono trasferiti al FAD, quindi passando attraverso un gruppo ferro-zolfo, all'ubiquinone. Da questo coenzima passano al complesso III e seguono il percorso precedentemente descritto.
L'energia rilasciata nella reazione di trasferimento degli elettroni al FAD non è sufficiente per guidare i protoni attraverso la membrana, quindi nessuna forza motrice del protone viene generata in questa fase della catena, e di conseguenza il FADH produce meno H+ che il NADH.
Accoppiamento o trasduzione di energia
L'energia generata nel processo di trasporto degli elettroni descritto in precedenza deve essere in grado di essere utilizzata per la produzione di ATP, una reazione catalizzata dall'enzima ATP sintasi o complesso V. La conservazione di questa energia è nota come accoppiamento energetico, e il meccanismo è stato difficile da caratterizzare.
Sono state descritte diverse ipotesi per descrivere questa trasduzione di energia. La migliore accettata è l'ipotesi di accoppiamento chemiosmotico, descritta di seguito..
Accoppiamento chemosmotico
Questo meccanismo propone che l'energia utilizzata per la sintesi di ATP provenga da un gradiente protonico nelle membrane cellulari. Questo processo interviene nei mitocondri, nei cloroplasti e nei batteri ed è legato al trasporto degli elettroni.
I complessi I e IV del trasporto di elettroni agiscono come pompe protoniche. Questi subiscono cambiamenti conformazionali che consentono loro di pompare protoni nello spazio intermembrana. Nel complesso IV, per ogni coppia di elettroni, due protoni vengono pompati fuori dalla membrana e altri due rimangono nella matrice, formando HDueO.
L'ubiquinone nel complesso III accetta protoni dai complessi I e II e li rilascia all'esterno della membrana. I complessi I e III consentono ciascuno il passaggio di quattro protoni per ogni coppia di elettroni trasportati.
La matrice mitocondriale ha una bassa concentrazione di protoni e un potenziale elettrico negativo, mentre lo spazio intermembrana presenta le condizioni inverse. Il flusso di protoni attraverso questa membrana rappresenta il gradiente elettrochimico che immagazzina l'energia necessaria (± 5 kcal / mol per protone) per la sintesi dell'ATP..
Sintesi di ATP
L'enzima ATP sintetasi è il quinto complesso coinvolto nella fosforilazione ossidativa. È responsabile dello sfruttamento dell'energia del gradiente elettrochimico per formare ATP.
Questa proteina transmembrana è costituita da due componenti: F0 e F1. Componente F0 permette il ritorno dei protoni alla matrice mitocondriale che funge da canale e la F1 catalizza la sintesi di ATP da ADP e Pio, utilizzando l'energia di detto ritorno.
Il processo di sintesi di ATP richiede un cambiamento strutturale in F1 e l'assemblaggio dei componenti F0 e F1. Traslocazione protonica attraverso F0 provoca cambiamenti conformazionali in tre subunità di F1, permettendogli di agire come un motore di rotazione, dirigendo la formazione di ATP.
La subunità responsabile del legame di ADP con Pio passa da uno stato debole (L) a uno attivo (T). Quando si forma l'ATP, una seconda subunità entra in uno stato aperto (O) che consente il rilascio di questa molecola. Dopo il rilascio di ATP, questa subunità passa dallo stato aperto a uno stato inattivo (L).
Molecole ADP e P.io legarsi a una subunità che è passata da uno stato O a uno stato L..
Prodotti
La catena di trasporto degli elettroni e la fosforilazione producono molecole di ATP. L'ossidazione del NADH produce circa 52,12 kcal / mol (218 kJ / mol) di energia libera.
La reazione complessiva per l'ossidazione del NADH è:
NADH + 1⁄2 ODue +H+ ↔ HDueO + NAD+
Trasferimento di elettroni da NADH e FADHDue avviene attraverso vari complessi, consentendo di suddividere la variazione di energia libera ΔG ° in "pacchetti" di energia più piccoli, che vengono accoppiati alla sintesi di ATP.
L'ossidazione di una molecola di NADH genera la sintesi di tre molecole di ATP. Mentre l'ossidazione di una molecola FADHDue si accoppia alla sintesi di due ATP.
Questi coenzimi derivano dai processi del ciclo della glicolisi e dell'acido citrico. Per ogni molecola di glucosio degradata, finiscono per produrre 36 o 38 molecole di ATP, a seconda della posizione delle cellule. 36 ATP è prodotto nel cervello e nel muscolo scheletrico, mentre 38 ATP è prodotto nel tessuto muscolare..
Caratteristiche
Tutti gli organismi, unicellulari e multicellulari, necessitano di energia minima nelle loro cellule per svolgere i processi al loro interno e, a loro volta, mantengono le funzioni vitali dell'intero organismo..
I processi metabolici richiedono energia per avere luogo. La maggior parte dell'energia utilizzabile è ottenuta dalla scomposizione di carboidrati e grassi. Questa energia è derivata dal processo di fosforilazione ossidativa.
Controllo della fosforilazione ossidativa
Il tasso di utilizzo dell'ATP nelle cellule controlla la sua sintesi e, a sua volta, a causa dell'accoppiamento della fosforilazione ossidativa con la catena di trasporto degli elettroni, regola generalmente anche la velocità di trasporto degli elettroni..
La fosforilazione ossidativa ha un controllo rigoroso che garantisce che l'ATP non venga generato più velocemente di quanto viene consumato. Ci sono alcune fasi nel processo di trasporto degli elettroni e fosforilazione accoppiata che regolano il tasso di produzione di energia..
Controllo coordinato della produzione di ATP
Le principali vie di produzione di energia (ATP cellulare) sono la glicolisi, il ciclo dell'acido citrico e la fosforilazione ossidativa. Il controllo coordinato di questi tre processi regola la sintesi di ATP.
Il controllo della fosforilazione mediante il rapporto di azione di massa dell'ATP dipende dal contributo preciso degli elettroni nella catena di trasporto. Questo a sua volta dipende dal [NADH] / [NAD+] che viene mantenuto elevato dall'azione della glicolisi e dal ciclo dell'acido citrico.
Questo controllo coordinato viene effettuato regolando i punti di controllo della glicolisi (PFK inibito dal citrato) e il ciclo dell'acido citrico (piruvato deidrogenasi, citrato tapease, isocitrato deidrogenasi e α-chetoglutarato deidrogenasi)..
Controllo da parte dell'accettatore
Il complesso IV (citocromo c ossidasi) è un enzima regolato da uno dei suoi substrati, cioè la sua attività è controllata dalla riduzione del citocromo c (cDue+), che a sua volta è in equilibrio con il rapporto di concentrazione tra [NADH] / [NAD+] e il rapporto di azione di massa di [ATP] / [ADP] + [Pio].
Maggiore è il rapporto [NADH] / [NAD+] e abbassare [ATP] / [ADP] + [Pio], maggiore è la concentrazione di citocromo [cDue+] e maggiore è l'attività del complesso IV. Questo viene interpretato, ad esempio, se confrontiamo organismi con diverse attività di riposo e attività elevata.
In un individuo con attività fisica elevata, il consumo di ATP e quindi la sua idrolisi ad ADP + Pio sarà molto alto, generando una differenza nel rapporto di azione della massa che provoca un aumento di [cDue+] e quindi un aumento della sintesi di ATP. In un individuo a riposo, si verifica la situazione inversa.
Infine, il tasso di fosforilazione ossidativa aumenta con la concentrazione di ADP all'interno dei mitocondri. Questa concentrazione dipende dai traslocatori ADP-ATP responsabili del trasporto di nucleotidi di adenina e Pio dal citosol alla matrice mitocondriale.
Agenti di disaccoppiamento
La fosforilazione ossidativa è influenzata da alcuni agenti chimici, che consentono al trasporto di elettroni di continuare senza che si verifichi la fosforilazione di ADP, disaccoppiando la produzione e la conservazione dell'energia.
Questi agenti stimolano il consumo di ossigeno dei mitocondri in assenza di ADP, provocando anche un aumento dell'idrolisi dell'ATP. Agiscono eliminando un intermediario o interrompendo uno stato energetico della catena di trasporto degli elettroni.
Il 2,4-dinitrofenolo, un acido debole che passa attraverso le membrane mitocondriali, è responsabile della dissipazione del gradiente protonico, poiché si legano ad essi sul lato acido e li rilasciano sul lato basico.
Questo composto è stato utilizzato come "pillola dimagrante" in quanto si è scoperto che produce un aumento della respirazione, quindi un aumento del tasso metabolico e conseguente perdita di peso. Tuttavia, è stato dimostrato che il suo effetto negativo potrebbe persino causare la morte.
La dissipazione del gradiente protonico produce calore. Le cellule del tessuto adiposo bruno utilizzano il disaccoppiamento controllato dagli ormoni per produrre calore. I mammiferi ibernati e i neonati privi di pelo sono costituiti da questo tessuto che funge da sorta di coperta termica..
Inibitori
I composti o gli agenti inibitori impediscono entrambi il consumo di ODue (trasporto di elettroni) come la fosforilazione ossidativa associata. Questi agenti prevengono la formazione di ATP utilizzando l'energia prodotta nel trasporto elettronico. Pertanto, la catena di trasporto si interrompe in quanto detto consumo di energia non è disponibile..
L'antibiotico oligomicina agisce come inibitore della fosforilazione in molti batteri, prevenendo la stimolazione dell'ADP alla sintesi dell'ATP.
Esistono anche agenti ionofori, che formano complessi liposolubili con cationi come K.+ e Na+, e passano attraverso la membrana mitocondriale con questi cationi. I mitocondri quindi utilizzano l'energia prodotta nel trasporto di elettroni per pompare cationi invece di sintetizzare ATP..
Riferimenti
- Alberts, B., Bray, D., Hopkin, K., Johnson, A., Lewis, J., Raff, M., Roberts, K. e Walter, P. (2004). Biologia cellulare essenziale. New York: Garland Science.
- Cooper, G. M., Hausman, R. E. & Wright, N. (2010). La cellula. (pagg. 397-402). Marban.
- Devlin, T. M. (1992). Libro di testo di biochimica: con correlazioni cliniche. John Wiley & Sons, Inc.
- Garrett, R. H. e Grisham, C. M. (2008). Biochimica. Thomson Brooks / Cole.
- Lodish, H., Darnell, J. E., Berk, A., Kaiser, C. A., Krieger, M., Scott, M. P. e Matsudaira, P. (2008). Biologia cellulare molecolare. Macmillan.
- Nelson, D.L. e Cox, M. M. (2006). Principi di biochimica di Lehninger 4a edizione. Ed Omega. Barcellona.
- Voet, D. e Voet, J. G. (2006). Biochimica. Panamerican Medical Ed..


Nessun utente ha ancora commentato questo articolo.