
Struttura, funzioni e malattie dell'acido sialico
Il acidi sialici sono monosaccaridi di nove atomi di carbonio. Appartengono alla famiglia dei derivati dell'acido neuraminico (acido 5-ammino-3,5-dideossi-D-glicero-D-galatto-nonulosonico) e sono ampiamente distribuiti in natura, in particolare nel regno animale.
Normalmente non si presentano come molecole libere, ma sono legate da legami α-glucosidici a molecole di carboidrati o altre molecole di acido sialico e possono quindi occupare posizioni terminali o interne all'interno di una catena di carboidrati lineare.
Il termine "acido sialico" è stato coniato per la prima volta da Gunnar Blix nel 1957, sebbene precedenti rapporti di altri ricercatori indicano che la sua scoperta risale a uno o due anni prima, quando erano descritti come parte delle glicoproteine sialo muciniche e sialo sialo sialo singolipidi (gangliosidi ).
Gli acidi sialici sono presenti in gran parte dei regni della natura. Sono stati rilevati in alcuni virus, batteri patogeni, protozoi, crostacei, vermi piatti, insetti e vertebrati come pesci, anfibi, uccelli e mammiferi. Al contrario, non sono stati trovati in funghi, alghe o piante..
Indice articolo
- 1 Struttura
- 2 funzioni
- 2.1 Ruolo nei processi di adesione cellulare
- 2.2 Ruolo nel tempo di vita dei componenti delle cellule del sangue
- 2.3 Ruoli nel sistema immunitario
- 2.4 Altre funzioni
- 3 malattie
- 4 Riferimenti
Struttura
Gli acidi sialici si trovano principalmente nella porzione terminale delle glicoproteine di superficie e dei glicolipidi, fornendo una grande diversità a questi glicoconiugati. I modelli differenziali di "sialilazione" sono prodotti dell'espressione di glicosiltransferasi tessuto-specifiche (sialiltransferasi).
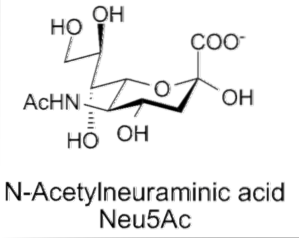
Strutturalmente, gli acidi sialici appartengono a una famiglia di circa 40 derivati naturali dell'acido neuraminico che sono N-acilati, dando origine a due strutture "parentali": acido N-acetilneuraminico (Neu5Ac) o acido N-glicolil neuraminico (Neu5Gc).
Le sue caratteristiche strutturali includono la presenza di un gruppo amminico (che può essere modificato) in posizione 5 e di un gruppo carbossilico in posizione 1, che può essere ionizzato a pH fisiologico. Un carbonio C-3 deossigenato e una molecola di glicerolo in posizione C-6.
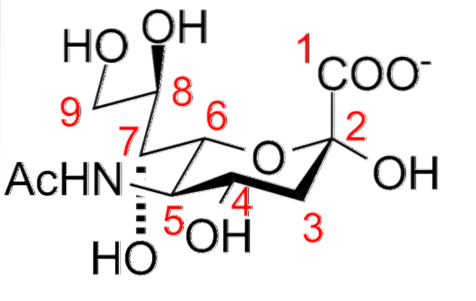
Molti derivati derivano dalla sostituzione dei gruppi idrossilici nelle posizioni C-4, C-7, C-8 e C-9 con porzioni di acetile, glicole, lattile, metile, solfato e fosfato; così come l'introduzione di doppi legami tra C-2 e C-3.
Nella posizione terminale lineare, l'attaccamento di una porzione di acido sialico a una catena oligosaccaridica comporta un legame α-glucosidico tra il gruppo idrossile del carbonio anomerico C-2 dell'acido sialico e i gruppi idrossilici dei carboni C-3, C- 4 o C-6 della porzione monosaccaridica.
Questi legami possono essere tra residui di galattosio, N-acetilglucosamina, N-acetilgalattosamina e in alcuni gangliosidi unici, glucosio. Possono verificarsi attraverso legami N-glicosidici o O-glicosidici.
Caratteristiche
Si ritiene che gli acidi sialici aiutino gli organismi parassiti a sopravvivere all'interno dell'organismo ospite; esempi di questo sono patogeni dei mammiferi che producono enzimi del metabolismo dell'acido sialico (sialidasi o liasi N-acetilneuraminiche).
Non esistono specie mammifere per le quali non sia stata segnalata la presenza di acidi sialici come parte delle glicoproteine in generale, glicoproteine sieriche, della mucosa, come parte delle strutture superficiali delle cellule o come parte dei carboidrati complessi.
Sono stati trovati negli oligosaccaridi acidi nel latte e nel colostro di esseri umani, bovini, pecore, cani e maiali, e anche come parte delle urine di ratti e umani..
Ruolo nei processi di adesione cellulare
I glicoconiugati con porzioni di acido sialico svolgono un ruolo importante nei processi di scambio di informazioni tra cellule vicine e tra le cellule e il loro ambiente..
La presenza di acido sialico nelle membrane cellulari contribuisce alla formazione di una carica negativa sulla superficie, che ha conseguenze positive in alcuni eventi di repulsione elettrostatica tra le cellule e alcune molecole..
Inoltre, la carica negativa conferisce agli acidi sialici nella membrana una funzione nel trasporto di ioni caricati positivamente..
È stato riportato che il legame dell'endotelio e dell'epitelio alla membrana basale glomerulare è facilitato dall'acido sialico, e questo influenza anche il contatto tra queste cellule..
Ruolo nella durata della vita dei componenti delle cellule del sangue
L'acido sialico ha importanti funzioni come parte della glicoforina A nella membrana plasmatica degli eritrociti. Alcuni studi hanno dimostrato che il contenuto di acido sialico è inversamente proporzionale all'età di queste cellule.
Gli eritrociti trattati con enzimi neuraminidasi, responsabili della degradazione dell'acido sialico, riducono drasticamente la loro emivita nel sangue da 120 giorni a poche ore. Lo stesso caso è stato osservato con le piastrine.
I trombociti perdono la loro capacità di adesione e aggregazione in assenza di acido sialico nelle loro proteine di superficie. Nei linfociti, l'acido sialico svolge anche un ruolo importante nei processi di adesione e riconoscimento cellulare, nonché nell'interazione con i recettori di superficie..
Funzioni nel sistema immunitario
Il sistema immunitario è in grado di distinguere tra strutture proprie o invasive in base al riconoscimento dei pattern di acido sialico presenti nelle membrane.
L'acido sialico, così come gli enzimi neuraminidasi e sialyltransferase, possiedono importanti proprietà regolatorie. Le porzioni terminali dell'acido sialico nei glicoconiugati della membrana plasmatica hanno funzioni di mascheramento o come recettori di membrana..
Inoltre, vari autori hanno sollevato la possibilità che l'acido sialico abbia funzioni antigeniche, ma non è ancora noto con certezza. Tuttavia, le funzioni di mascheramento dei residui di acido sialico sono molto importanti nella regolazione cellulare..
La mascheratura può avere un ruolo protettivo diretto o indiretto, a seconda che la porzione di acido sialico ricopra direttamente il residuo di carboidrato antigenico, oppure sia un acido sialico in un glicoconiugato adiacente a mascherare la porzione antigenica..
Alcuni anticorpi possiedono residui Neu5Ac che mostrano proprietà neutralizzanti il virus, poiché queste immunoglobuline sono in grado di prevenire l'adesione dei virus solo a coniugati (glicoconiugati con porzioni di acido sialico) sulla membrana cellulare.
Altre funzioni
Nel tratto intestinale gli acidi sialici svolgono un ruolo altrettanto importante, poiché fanno parte delle mucine, che hanno proprietà lubrificanti e protettive, essenziali per tutto l'organismo..
Inoltre, gli acidi sialici sono presenti anche nelle membrane delle cellule epiteliali bronchiali, gastriche e intestinali, dove sono coinvolti nel trasporto, nella secrezione e in altri processi metabolici..
Malattie
È noto che numerose malattie comportano anomalie nel metabolismo dell'acido sialico e queste sono note come sialidosi. Tra i più importanti ci sono la sialuria e la malattia di Salla, che sono caratterizzate da escrezione urinaria con grandi quantità di acidi sialici liberi.
Altre malattie di ordine immunologico hanno a che fare con alterazioni degli enzimi anabolici e catabolici legati al metabolismo dell'acido sialico, che provocano un accumulo aberrante di glicoconiugati con porzioni di acido sialico..
Sono note anche alcune malattie legate ai fattori del sangue, come la trombocitopenia, che consiste in una diminuzione del livello dei trombociti nel sangue, probabilmente causata dalla mancanza di acido sialico nella membrana..
La malattia di Von Willebrand corrisponde a un difetto nella capacità dei trombociti di aderire ai glicoconiugati della membrana subendoteliale della parete dei vasi sanguigni, causato da carenze o carenze nella glicosilazione o sialilazione.
La trombastenia di Glanzmann è un altro disturbo congenito dell'aggregazione dei trombociti la cui radice è la presenza di glicoproteine difettose nella membrana dei trombociti. È stato dimostrato che i difetti di queste glicoproteine sono associati a un contenuto ridotto di Neu5Ac.
Riferimenti
- Clayden, J., Greeves, N., Warren, S. e Wothers, P. (2001). Chimica organica (1a ed.). New York: Oxford University Press.
- Demchenko, A. V. (2008). Manuale di glicosilazione chimica: progressi nella stereoselettività e rilevanza terapeutica. Wiley-VCH.
- Rosenberg, A. (1995). Biologia degli acidi sialici. New York: Springer Science + Business Media, LLC.
- Schauer, R. (1982). Acidi sialici: chimica, metabolismo e funzione. Springer-Verlag Wien New York.
- Traving, C., & Schauer, R. (1998). Struttura, funzione e metabolismo degli acidi sialici. CMLS Scienze della vita cellulare e molecolare, 54, 1330-1349.



Nessun utente ha ancora commentato questo articolo.