
Struttura chimica, proprietà e usi di Tusfrano
Il tusfrano È un elemento chimico radioattivo che appartiene al gruppo 13 (IIIA) e al periodo 7 della tavola periodica. Non si ottiene in natura, o almeno non in condizioni terrestri. La sua emivita è solo di circa 38 ms a un minuto; quindi, la sua grande instabilità lo rende un elemento molto sfuggente.
In effetti, era così instabile all'alba della sua scoperta che la IUPAC (International Union of Pure and Applied Chemistry) non ha fornito una data precisa per l'evento in quel momento. Per questo motivo la sua esistenza come elemento chimico non è stata ufficializzata ed è rimasta all'oscuro..
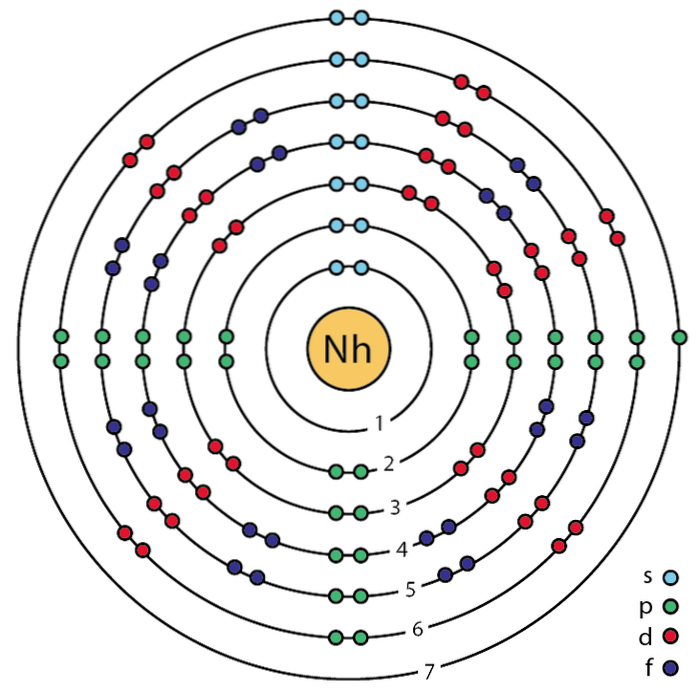
Il suo simbolo chimico è Tf, la massa atomica è 270 g / mol, ha una Z uguale a 113 e una configurazione di valenza [Rn] 5f146d107sDue7p1. Inoltre, i numeri quantici del suo elettrone differenziale sono (7, 1, -1, +1/2). L'immagine sopra mostra il modello di Bohr per l'atomo di tusfrano..
Questo atomo era precedentemente noto come ununtrium, e oggi è stato ufficializzato con il nome Nihonium (Nh). Nel modello puoi controllare, come un gioco, gli elettroni dei gusci interni e di valenza per l'atomo di Nh.
Indice articolo
- 1 Scoperta del tusfrano e ufficializzazione del nihonium
- 1.1 Nihonium
- 2 Struttura chimica
- 3 Proprietà
- 3.1 Punto di fusione
- 3.2 Punto di ebollizione
- 3.3 Densità
- 3.4 Entalpia di vaporizzazione
- 3.5 Raggio covalente
- 3.6 stati di ossidazione
- 4 Usi
- 5 Riferimenti
Scoperta del tusfrano e ufficializzazione del nihonium
Un team di scienziati del Lawrence Livermore National Laboratory, negli Stati Uniti, e un gruppo di Dubna, in Russia, sono stati quelli che hanno scoperto tusfrano. Questa scoperta è avvenuta tra il 2003 e il 2004.
D'altra parte, i ricercatori del Riken Laboratory, in Giappone, sono riusciti a sintetizzarlo, essendo il primo elemento sintetico prodotto in quel paese..
È stato derivato dal decadimento radioattivo dell'elemento 115 (unumpentium, Uup), nello stesso modo in cui gli attinidi sono prodotti dal decadimento dell'uranio.
Prima della sua accettazione ufficiale come nuovo elemento, la IUPAC lo chiamò provvisoriamente ununtrium (Uut). Ununtrium (Ununtrium, in inglese) significa (uno, uno, tre); cioè 113, che è il suo numero atomico scritto in unità.
Il nome ununtrio era dovuto ai regolamenti IUPAC del 1979. Tuttavia, secondo la nomenclatura di Mendeleev per elementi ancora da scoprire, il suo nome doveva essere Eka-tallio o dvi-indiano..
Perché tallio e indio? Perché sono gli elementi del gruppo 13 più vicini ad esso e, quindi, dovrebbe condividere con loro alcune somiglianze fisico-chimiche.
Nihonium
Ufficialmente, è accettato che provenga dal decadimento radioattivo dell'elemento 115 (moscovio), avente il nome Nihonium, con il simbolo chimico di Nh.
"Nihon" è un termine usato per designare il Giappone, presentando così il suo nome nella tavola periodica.
Nelle tavole periodiche precedenti al 2017 compaiono tusfrano (Tf) e unumpentium (Uup). Tuttavia, nella stragrande maggioranza delle tavole periodiche di prima dell'ununtrium sostituisce il tusfrano.
Attualmente Nihonium occupa il posto di Tusfrano nella tavola periodica e Muscovium sostituisce anche Unumpentium. Questi nuovi elementi completano il periodo 7 con tenesin (Ts) e oganesón (Og).
Struttura chimica
Man mano che si scende attraverso il gruppo 13 della tavola periodica, la famiglia della terra (boro, alluminio, gallio, indio, tallio e tusfrano), il carattere metallico degli elementi aumenta..
Il tusfrano è quindi l'elemento del gruppo 13 con il maggior carattere metallico. I suoi atomi voluminosi devono adottare alcune delle possibili strutture cristalline, tra cui: bcc, ccp, hcp e altre.
Quale di questi? Questa informazione non è ancora disponibile. Tuttavia, una congettura sarebbe quella di ipotizzare una struttura poco compatta e una cella unitaria di volume maggiore di quella cubica..
Proprietà
Poiché è un elemento sfuggente e radioattivo, molte delle sue proprietà sono previste e quindi non ufficiali..
Punto di fusione
700K.
Punto di ebollizione
1400K.
Densità
16 Kg / m3
Entalpia di vaporizzazione
130 kJ / mol.
Raggio covalente
136 pm.
Stati di ossidazione
+1, +3 e +5 (come il resto degli elementi del gruppo 13).
Dal resto delle loro proprietà, ci si può aspettare che mostrino comportamenti simili a quelli dei metalli pesanti o di transizione..
Applicazioni
Date le sue caratteristiche, le applicazioni industriali o commerciali sono nulle, quindi viene utilizzato solo per la ricerca scientifica.
In futuro la scienza e la tecnologia potrebbero trarre alcuni vantaggi appena rivelati. Forse, per elementi estremi e instabili come il nihonium, i suoi possibili usi ricadono anche in scenari estremi e instabili per i tempi presenti..
Inoltre, i suoi effetti sulla salute e sull'ambiente non sono ancora stati studiati a causa della sua limitata durata. Per questo motivo, non è nota alcuna possibile applicazione in medicina o il grado di tossicità..
Riferimenti
- Ahazard.sciencewriter. 113 nihonium (Nh) modello Bohr migliorato. (2016, 14 giugno). [Figura]. Estratto il 30 aprile 2018 da: commons.wikimedia.org
- Royal Society of Chemistry. (2017). Nihonium. Estratto il 30 aprile 2018 da: rsc.org
- Tim Sharp. (1 dicembre 2016). Fatti sul Nihonium (elemento 113). Estratto il 30 aprile 2018 da: livescience.com
- Lulia Georgescu. (24 ottobre 2017). Nihonium l'oscuro. Estratto il 30 aprile 2018 da: nature.com
- The Editors of Encyclopaedia Britannica. (2018). Nihonium. Estratto il 30 aprile 2018 da: britannica.com


Nessun utente ha ancora commentato questo articolo.