
Proprietà fisiche e chimiche dell'acqua

Il proprietà fisiche e chimiche dell'acqua Sono tutte quelle manifestazioni dell'acqua che possiamo misurare grazie alle interazioni delle sue molecole con se stesse o con l'ambiente circostante. Ma cos'è l'acqua? L'acqua è una sostanza chimica o una molecola formata dall'unione di un atomo di ossigeno (O) con due atomi di idrogeno (H).
Questi tre atomi sono tenuti insieme dalla formazione di legami covalenti, legami di tipo molto forti e stabili. La molecola d'acqua ha la formula H.DueOppure può essere scritto come H-O-H. È questa molecola, i suoi legami e le loro interazioni che sono responsabili del fatto che sia una sostanza liquida incolore e insapore..

L'acqua è distribuita in gran parte sulla Terra, tra l'acqua dolce e quella salata. L'acqua è essenziale per l'esistenza della vita sul nostro pianeta, poiché è una risorsa naturale molto preziosa. Si trova tra il 60 e il 70% negli organismi viventi, una percentuale elevata che consente loro di svolgere innumerevoli funzioni.
Alcune di queste funzioni vitali includono strutturali, regolatorie, come il mantenimento della temperatura corporea e la regolazione del pH (acidità o alcalinità) entro limiti normali. Allo stesso modo, l'acqua effettua il trasporto di sostanze nutritive e rifiuti negli esseri viventi.
Viene inoltre utilizzato in molti settori della routine produttiva, tecnologica, scientifica e quotidiana dell'essere umano; dalla pulizia, la cottura del cibo, tra gli altri usi.
Indice articolo
- 1 Proprietà fisiche dell'acqua
- 1.1 Gusto
- 1.2 Aspetto
- 1.3 Stati dell'acqua
- 1.4 Densità
- 1.5 Punto di congelamento
- 1.6 Punto di ebollizione
- 1.7 Conducibilità elettrica
- 1.8 Coesione
- 1.9 Adesione
- 1.10 Tensione superficiale
- 1.11 Capillarità
- 1.12 Azione solvente
- 2 Proprietà chimiche dell'acqua
- 2.1 Natura chimica
- 2.2 Polarità
- 2.3 Ionizzazione
- 2.4 Capacità reattiva
- 2,5 pH
- 2.6 Anfoterismo
- 3 Riferimenti
Proprietà fisiche dell'acqua
Le proprietà fisiche dell'acqua sono correlate alle caratteristiche o alle grandezze che possono essere misurate o determinate quando si considera la materia, come la sua massa, energia, tra gli altri..
Tra le grandezze fisiche dell'acqua ci sono il suo colore, l'odore, le forme in cui può essere trovata e tutte quelle che possiamo determinare senza produrre reazioni o alterare la sua composizione chimica..
Gusto
Quando assaggiamo un po 'd'acqua pura, il nostro palato scopre che è insapore o insapore. È anche inodore o inodore. A causa del processo di purificazione, a volte è possibile percepire un leggero odore dovuto ai residui di cloro. Sono i minerali che conferiscono all'acqua diverse carte di sapore.
Aspetto

L'acqua in generale è incolore e trasparente se vista in un bicchiere di vetro. Tuttavia, sembra avere un leggero colore azzurro quando accumulato in grandi quantità in grandi contenitori o quando osservato su ghiacciai, fiumi o mari..
Ed è che infatti l'acqua presenta una certa colorazione bluastra pallida, la cui percezione è concentrata quanto maggiore è la quantità di acqua..
Stati dell'acqua
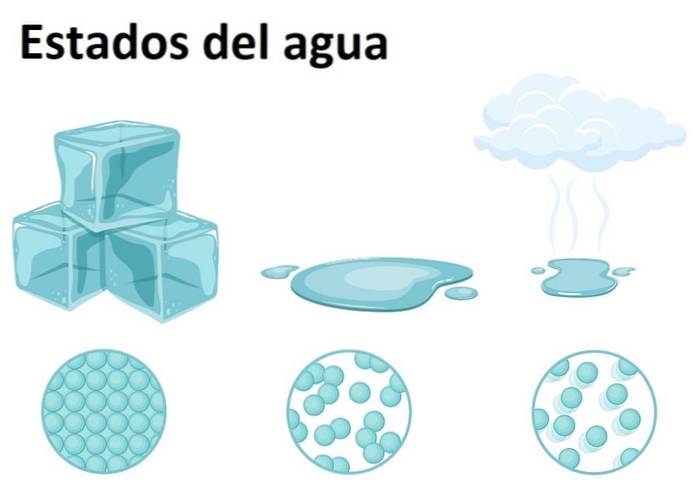
L'acqua è molto abbondante sulla Terra e può essere trovata in uno qualsiasi dei tre stati della materia: solido, liquido o gassoso. L'acqua a temperatura ambiente è una sostanza liquida, che corrisponde alla sua forma più comune.
In quanto solido, l'acqua si chiama ghiaccio o neve, a seconda delle dimensioni dei suoi cristalli e del processo di formazione. Nel frattempo, lo stato gassoso si forma quando l'acqua passa da uno stato liquido a uno gassoso, formando il famoso vapore acqueo, facilmente riconoscibile in cucina e sopra il cibo..
Densità
La densità dell'acqua pura è di circa 1 g / cm3. Nel frattempo, la densità dell'acqua di mare è un po 'più alta a causa del sale che contiene..
Punto di congelamento
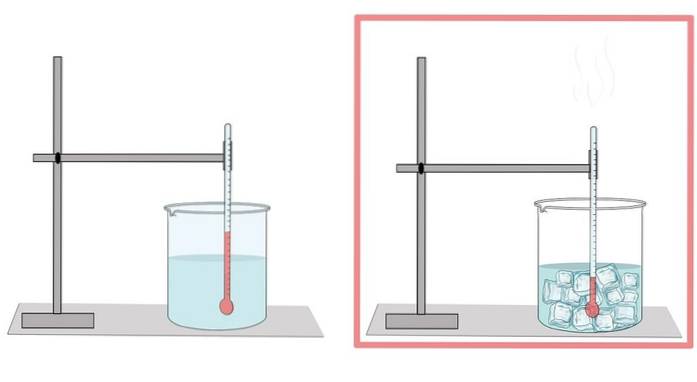
L'acqua gela a 0 ° C. A questa temperatura passa dalla fase liquida alla fase solida. Quando l'acqua si congela, si espande. Questo è il motivo per cui nella sua forma solida ha una densità inferiore rispetto allo stato liquido, il che rende più facile il galleggiamento del ghiaccio sull'acqua liquida..
Inoltre, questo è il motivo per cui quando l'acqua in una bottiglia si raffredda, non dovrebbe essere riempita molto, poiché il ghiaccio si espande e finisce per rompere la bottiglia..
Punto di ebollizione
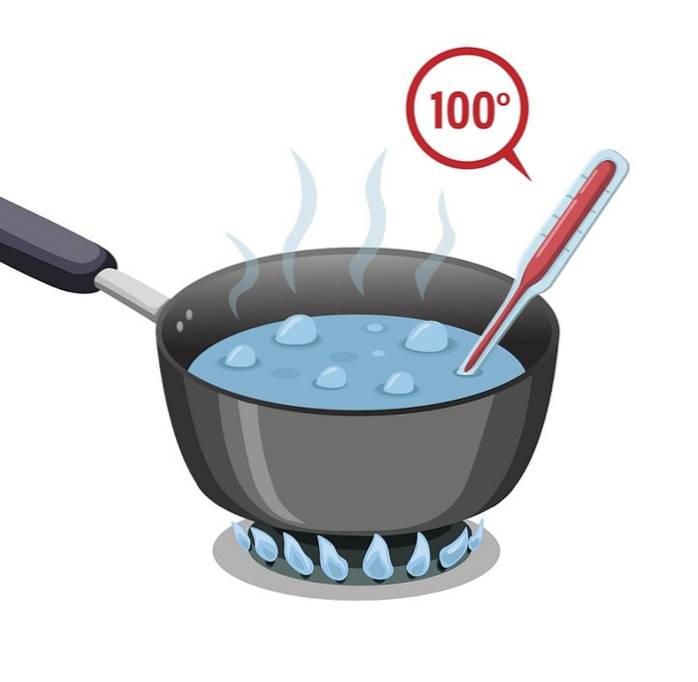
L'acqua ha un alto punto di ebollizione che è di 100 ° C. Deve essere sottoposto a molto calore in modo che possa riscaldarsi e bollire o raggiungere il punto di ebollizione.
L'acqua ha quindi un elevato calore specifico, o anche chiamato capacità termica, che le fa impiegare tempo per riscaldarsi; ma anche in raffreddamento, cioè, il processo necessario per perdere il calore acquisito è lento.
Questa proprietà lo rende molto utile nei sistemi di refrigerazione, nei sistemi di regolazione della temperatura corporea, tra gli altri correlati.
Conduttività elettrica
L'acqua è un buon conduttore di elettricità. Non importa quanto sia pura l'acqua, avrà sempre una certa quantità di ioni, che le conferisce la proprietà di avere una delle costanti dielettriche più elevate tra i liquidi non metallici..
Coesione
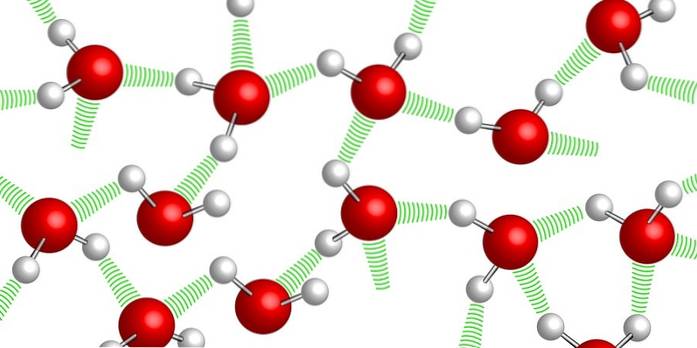
Le molecole d'acqua sono tenute insieme grazie ai cosiddetti legami idrogeno: legami deboli che si instaurano tra una e l'altra molecola d'acqua. A causa di questo alto livello di coesione è molto difficile comprimere l'acqua.
Adesione

È facile che l'acqua aderisca, ad esempio, alla superficie molto pulita di un vetro, formando una pellicola, che chiamiamo umidità o "bagnata". Inoltre, l'acqua aderisce rapidamente alla nostra pelle, quindi ci bagniamo non appena piove o entriamo in una piscina. Altrimenti saremmo asciutti in pochi secondi.
Tensione superficiale
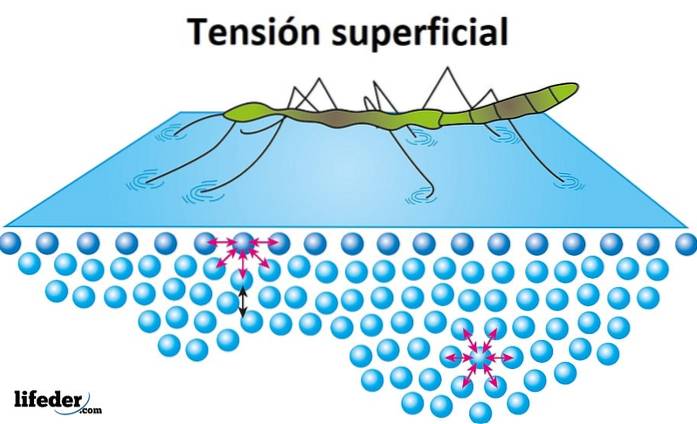
La tensione superficiale è la resistenza offerta dal liquido sulla sua superficie da penetrare. L'acqua ha un'elevata tensione superficiale, un prodotto della coesione che esiste tra le sue molecole, che le fa formare facilmente gocce invece di diffondersi liberamente su una superficie liscia..
La tensione superficiale è evidente quando gli insetti sembrano muoversi o camminare sull'acqua senza affondare, ed è il motivo per cui alcune foglie o altri oggetti leggeri possono galleggiare sull'acqua.
Capillarità

La facilità con cui l'acqua si muove su o giù per un tubo capillare descrive la proprietà capillare dell'acqua. Questa proprietà è anche dovuta alle elevate proprietà di coesione e adesione dell'acqua..
La capillarità è utilizzata dalla natura vegetale per fornire acqua alle foglie dei rami più alti di un albero, oltre a facilitarne l'assorbimento da parte delle radici delle piante..
Allo stesso modo, le proprietà della tensione superficiale e della capillarità significano che l'acqua è una parte strutturale delle cellule, che fa parte del sangue e che scorre o scorre facilmente attraverso i diversi vasi sanguigni..
Azione solvente

L'acqua può dissolvere molte sostanze, il che è vitale per gli organismi viventi, poiché tutte le reazioni chimiche negli esseri viventi avvengono in un mezzo acquoso. Negli organismi viventi serve a trasportare nutrienti, ioni e molte altre sostanze.
Serve anche a trasportare i rifiuti, come l'urea, che viene eliminata nell'acqua dalle urine. Quando una sostanza si dissolve e si miscela bene con l'acqua, si dice che sia idrofila o solubile in acqua. Se non si miscela o si dissolve bene, la sostanza si dice che sia idrofobica o insolubile in acqua.
Proprietà chimiche dell'acqua
Le proprietà o le caratteristiche chimiche sono quelle che si verificano quando si verificano cambiamenti nella struttura chimica dell'acqua. È quindi importante dare una breve occhiata alla sua struttura molecolare..
Natura chimica
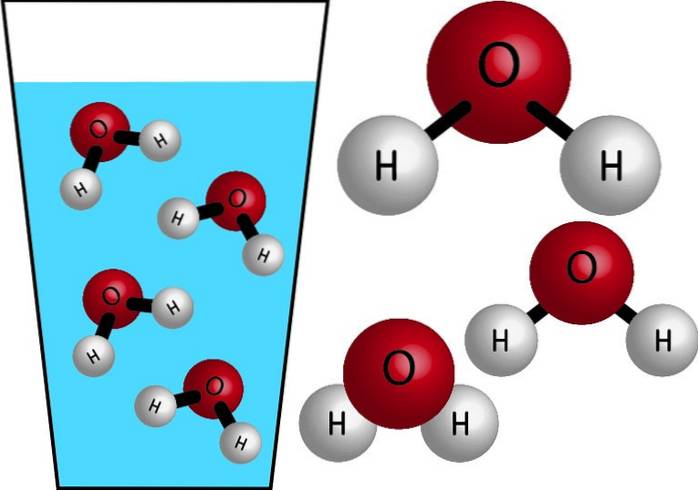
L'acqua è una molecola inorganica, perché non contiene C (carbonio) e la sua formula chimica è H.DueO. I loro atomi si uniscono condividendo elettroni, formando legami covalenti, legami forti e molto stabili. La sua massa molare è di 18 g / mol, cioè una mole di acqua ha una massa di 18 grammi.
Polarità
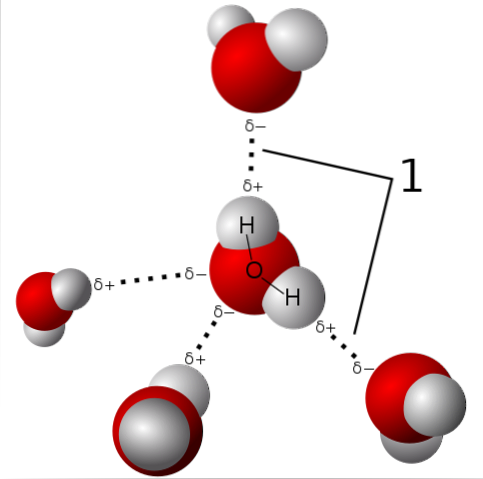
La molecola d'acqua è neutra, ma ha una certa polarità, perché la condivisione dei suoi elettroni non è così equa.
Poiché l'ossigeno attrae gli elettroni condivisi verso se stesso con più forza, la molecola d'acqua rimane da questo lato dove si trova l'ossigeno, con la tendenza ad avere una certa carica negativa; e quindi viene lasciata con una carica parziale positiva verso dove si trovano gli idrogeni (vedi immagine in alto).
Questa polarità facilita l'unione delle molecole d'acqua tra loro e l'unione dell'acqua con altre molecole che hanno anche differenze di carica nella loro struttura, il che promuove le proprietà fisiche descritte nelle sezioni precedenti..
Ionizzazione
Spontaneamente in acqua liquida c'è una leggera ionizzazione o auto-dissociazione. Significa che alcune delle sue molecole vengono riorganizzate modificando la loro normale struttura molecolare, generando nuove molecole caricate elettricamente, come gli ioni idronio (H3O+) e idrossile (OH-).
Capacità reattiva
L'acqua reagisce con molte sostanze, formando una grande diversità di composti chimici. Per elettrolisi, l'acqua può decomporsi, separando l'ossigeno dai suoi due idrogeni. Questo processo si verifica quando una corrente elettrica passa attraverso l'acqua. Anche l'acqua nella sua forma solida può anche far parte di alcune reazioni chimiche.
pH

L'acqua pura ha un pH neutro (pari a 7), mentre l'acqua di mare è leggermente alcalina (maggiore di 7). L'acqua piovana diventa leggermente acida (pH inferiore a 7) quando si mescola con componenti presenti nell'atmosfera, come anidride carbonica o CO.Due, per esempio.
Anfoterismo
L'acqua è anfotera, cioè può comportarsi come un acido o come una base a seconda del pH della soluzione. Questa proprietà chimica supporta il suo ruolo di regolatore del pH..
Riferimenti
- Shiver & Atkins. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). CENGAGE Apprendimento.
- Castillero M. O. (2020). Psicologia e mente. Le 15 proprietà fisiche e chimiche dell'acqua. Estratto da: psicologiaymente.com
- Wikipedia (2020). Proprietà dell'acqua. Estratto da: en.wikipedia.org
- Sharp K. A. (s.f.). Acqua: struttura e proprietà. Recupero da: crystal.med.upenn.edu
- BYJU'S. (s.f.). Proprietà fisiche e chimiche dell'acqua. Estratto da: byjus.com
- Energia e ambiente scolastici. (s.f.). L'acqua era una risorsa. Estratto da: eniscuola.net



Nessun utente ha ancora commentato questo articolo.