
Caratteristiche, struttura, funzioni dei lipolisaccaridi
Il lipopolisaccaridi (LPS) sono i componenti più importanti della parete cellulare dei batteri gram-negativi (75% della superficie). Gli LPS sono combinazioni complesse di lipidi e carboidrati che sono molto importanti per mantenere la vitalità e la sopravvivenza dei batteri.
Queste sostanze batteriche, chiamate anche endotossine, si distribuiscono in tutti gli ambienti, dai batteri presenti nel suolo, nell'aria, nell'acqua e nei cibi animali. Sono invece presenti nella flora batterica intestinale, vaginale e orofaringea, contaminando una grande varietà di prodotti dell'uomo..
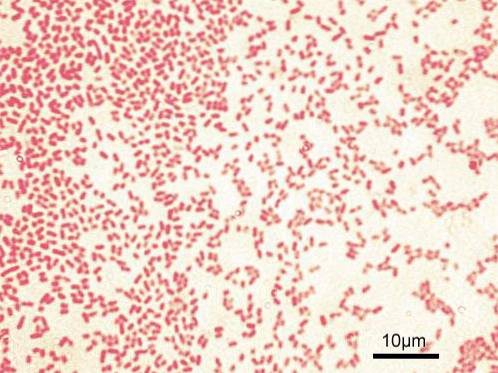
Si noti inoltre che i lipopolisaccaridi sono potenti induttori di sostanze pro-infiammatorie come citochinine, radicali liberi e prodotti derivati dall'acido arachidonico..
Indice articolo
- 1 Caratteristiche
- 2 Struttura
- 3 tipi di LPS
- 4 funzioni
- 4.1 LPS nella risposta immunitaria
- 4.2 Patologie che innescano LPS
- 5 Riferimenti
Caratteristiche
Gli LPS sono sostanze piuttosto complesse con pesi molecolari elevati, che variano chimicamente tra i vari gruppi di batteri gram-negativi. Sono molto legati ai leucociti, in questo modo quando entrano nel sangue vi aderiscono, il bersaglio principale sono i macrofagi.
La produzione di citochinine in eccesso può causare gravi condizioni cliniche come sepsi e shock settico. Inoltre, gli LPS sono coinvolti nella modellazione della fisiopatologia di altre malattie come la sindrome emolitica uremica..
Gli LPS sono responsabili di causare reazioni infiammatorie violente negli esseri umani, motivo per cui sono tossine presenti all'interno del corpo (endotossine).
In generale, i lipolisaccaridi non entrano nel sistema circolatorio attraverso l'intestino a causa delle giunzioni strette che formano l'epitelio intestinale. Ma quando queste unioni sono compromesse, c'è permeabilità intestinale, provocano danni e accelerano i processi infiammatori.
Gli LPS hanno azione immunogenica ed endotossica e partecipano all'attivazione del sistema immunitario e alla mediazione dell'aderenza ai batteri. Inoltre, rappresentano un fattore di virulenza che contribuisce al processo patogeno e all'evasione della risposta immunitaria..
Struttura
Per quanto riguarda la loro struttura, si può dire che siano molecole eterogenee, poiché sono costituite da una regione idrofila costituita da polisaccaridi e da una lipofila chiamata lipide A.
Il primo, è il più esterno rispetto al corpo del batterio, costituito da una grande quantità di polisaccaridi ramificati, anch'essi complessi e molto specifici per la specie di batterio, noto anche come antigene O. Segue uno strato di polisaccaridi meno complessi, chiamati "core" o nucleo di oligosaccaridi.
Quest'ultimo, nella sua regione più esterna, presenta zuccheri comuni come D-glucosio, D-Galattosio, N-acetil D-glucosamina e N-acetil D-galattosamina e la sua parte interna con zuccheri meno comuni come eptosi.
Questa regione polisaccaridica si lega alla porzione lipidica della molecola (Lipide A) attraverso l'acido 3-cheto-2-dexocioctonico (Kdo). Inoltre, il lipide A è legato in modo covalente alla membrana esterna.
La regione del lipide A è costituita da un disaccaride generalmente bifosforilato, acilato con sei acidi grassi che possono avere da 12 a 14 atomi di carbonio. Questo è riconosciuto in modo specifico e sensibile dai componenti dell'immunità innata (fagociti) e rappresenta il centro immunoreattivo dell'LPS e un fattore di virulenza..
Tipi di LPS
Esistono LPS che contengono nella loro struttura le suddette regioni, la porzione di lipide A, un nucleo di oligosaccaridi e l'antigene O, si chiamano LPS S o lipopolisaccaridi lisci.
Quelli in cui l'antigene O è assente sono invece chiamati LPS R o lipolisaccaridi ruvidi o anche lipo-oligosaccaridi..
Caratteristiche
La funzione principale dell'LPS nei batteri è fornire una certa resistenza alla digestione da parte della bile della cistifellea. Gli LPS, sebbene chimicamente diversi dai fosfolipidi, hanno caratteristiche fisiche simili; in questo modo possono partecipare allo stesso modo alla formazione di una membrana.
Sebbene gli LPS non abbiano tossicità da soli, l'effetto tossico è causato dal loro legame con monociti o macrofagi del sistema endoteliale del reticolo. Ciò provoca la sintesi e il rilascio di varie sostanze con caratteristiche proinfiammatorie..
Queste sostanze includono fattore di necrosi tumorale (TNF-α), interleuchine I-L1, I-L8, IL-12, IL-18, interferone-gamma (IFN-γ, fattore di attivazione delle piastrine e diverse chemochine Questi effetti sono causati anche a livello epiteliale , cellule muscolari endoteliali e lisce con effetti più conservati..
Gli LPS sono potenti attivatori della coagulazione intravascolare e delle vie classiche e alternative del sistema del complemento e della secrezione di sottoprodotti dell'acido arachidonico, come le prostaglandine..
Inoltre sensibilizzano altre cellule abbassando le soglie di attivazione verso vari agonisti che inducono il rilascio di radicali liberi come quelli privi di ossigeno e azoto, IFN-γ, tra gli altri..
LPS nella risposta immunitaria
LPS attiva la risposta immunitaria innata che è prodotta solo dall'interazione LPS-ospite, mettendo in moto importanti meccanismi come la fagocitosi mediata da polimorfi nucleari (neutrofili) e macrofagi..
D'altra parte interviene nei processi che generano l'infiammazione, inducendo sostanze proinfiammatorie e attivando il sistema del complemento mediato dalla via alternativa. Se questa risposta immunitaria innata non è sufficiente, viene attivata la risposta immunitaria cellulare e umorale..
Il riconoscimento e la segnalazione di LPS avviene quando vengono rilasciati dalla parete batterica, che può verificarsi quando il batterio muore o attraverso la proteina LBP (proteina legante i lipopolisaccaridi).
LBP, che è una proteina plasmatica (transferasi lipidica), forma complessi LPS-LBP nel sangue. Quindi questa proteina trasferisce l'LPS alla molecola CD14, che è l'unica responsabile del riconoscimento dell'LPS e della mediazione della sua funzione biologica..
Il CD14 può essere una proteina solubile nel sangue o ancorato alla membrana delle cellule che esprimono TLR4 (recettore), dove rinunciano a LPS perché il CD14 non può attraversare la membrana e raggiungere il citoplasma. Ciò impedirà solo la generazione della risposta LPS..
Patologie che innescano LPS
LPS viene utilizzato in laboratorio per lo studio di varie condizioni come l'Alzheimer, la sclerosi multipla, le condizioni infiammatorie intestinali, il diabete e persino l'autismo, grazie alla sua capacità di provocare rapidamente reazioni infiammatorie. Nei pazienti con queste malattie, i livelli di lipolisaccaridi nel sangue sono alti..
Una volta che TLR4 trasduce i segnali di attività LPS, la co-espressione di proteine correlate a TLR4 come MD-2, contribuisce ad ottimizzare il segnale, formando un complesso.
Questo complesso favorisce l'attivazione di un'ampia rete di proteine citoplasmatiche e il reclutamento della proteina di differenziazione mieloide 88. Ciò genera la traslocazione di fattori di trascrizione come IRF3 e NF-KB, che partecipano all'espressione di geni legati alla produzione di citochinine, chemochine e molecole di attivazione.
Tutto ciò porta ad una forte reazione infiammatoria, attivazione cellulare e meccanismi regolatori mediati da IL-10. LPS in alte concentrazioni può causare febbre, aumento della frequenza cardiaca e persino shock settici.
Riferimenti
- Cabello, R. R. (2007). Microbiologia e parassitologia umana / Microbiologia e parassitologia umana: basi eziologiche delle malattie infettive e parassitarie / Base eziologica delle malattie infettive e parassitarie. Panamerican Medical Ed..
- Hall, J. E. (2011). Libro di testo di Guyton e Hall di fisiologia medica. Elsevier Health Sciences.
- Knirel, Y. A., e Valvano, M. A. (a cura di). (2011). Lipopolisaccaridi batterici: struttura, sintesi chimica, biogenesi e interazione con le cellule ospiti. Springer Science & Business Media.
- Nelson, D.L. e Cox, M. M. (2006). Principi di biochimica di Lehninger. 4a edizione. Ed Omega. Barcellona (2005).
- Rabinovich, G. A. (2004). Immunopatologia molecolare: nuove frontiere della medicina: un legame tra ricerca biomedica e pratica clinica. Panamerican Medical,
- Stanier, R. Y. e Villanueva, J. R. (1996). Microbiologia. Invertito.

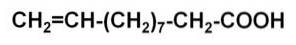

Nessun utente ha ancora commentato questo articolo.