
Proprietà ed esempi degli idrocarburi insaturi

Il idrocarburi insaturi sono quelli che contengono almeno un doppio legame di carbonio nella loro struttura, potendo contenere un triplo legame poiché la saturazione di una catena significa che ha ricevuto tutti i possibili atomi di idrogeno in ogni carbonio, e non ci sono coppie di elettroni liberi dove possono entrare più idrogeni.
Gli idrocarburi insaturi si dividono in due tipi: alcheni e alchini. Gli alcheni sono composti idrocarburici che hanno uno o più doppi legami all'interno della loro molecola. Nel frattempo, gli alchini sono composti idrocarburici che hanno uno o più tripli legami all'interno della loro formula..
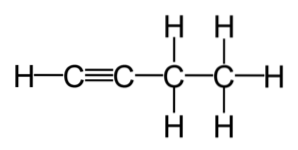
Gli alcheni e gli alchini sono usati frequentemente in commercio. Si tratta di composti con un livello di reattività superiore a quello degli idrocarburi saturi, il che li rende il punto di partenza di molte reazioni, generate dai più comuni alcheni e alchini..
Indice articolo
- 1 Nomenclatura
- 1.1 Nomenclatura degli alcheni
- 1.2 Nomenclatura degli alchini
- 2 Proprietà
- 2.1 Doppi e tripli legami
- 2.2 isomerizzazione cis-trans
- 2.3 Acidità
- 2.4 Polarità
- 2.5 Punti di ebollizione e di fusione
- 3 esempi
- 3.1 Etilene (C2H4)
- 3.2 Etina (C2H2)
- 3.3 Propilene (C3H6)
- 3.4 Ciclopentene (C5H8)
- 4 Articoli di interesse
- 5 Riferimenti
Nomenclatura
Gli idrocarburi insaturi sono denominati in modo diverso a seconda che siano alcheni o alchini, utilizzando i suffissi "-eno" e "-ino".
Gli alcheni hanno almeno un doppio legame carbonio-carbonio nella loro struttura e hanno la formula generale CnH2n, mentre gli alchini contengono almeno un triplo legame e sono gestiti dalla formula CnH2n-2.
Nomenclatura degli alcheni
Per denominare gli alcheni, devono essere indicate le posizioni dei doppi legami carbonio-carbonio. I nomi dei composti chimici che contengono legami C = C terminano con il suffisso "-eno".
Come con gli alcani, il nome del composto di base è determinato dal numero di atomi di carbonio nella catena più lunga. Ad esempio, la molecola CHDue= CH-CHDue-CH3 sarà chiamato "1-butene", ma quello di H3C-CH = CH-CH3 si chiamerà "2-butene".
I numeri che si osservano nei nomi di questi composti indicano l'atomo di carbonio con il numero più piccolo nella catena in cui si trova il legame C = C dell'alchene..
Il numero di atomi di carbonio in questa catena identifica il prefisso del nome, simile agli alcani ("met-", "et-", "pro", "but-", ecc.), Ma sempre utilizzando il suffisso "-eno ".
Va inoltre specificato se la molecola è cis o trans, che sono tipi di isomeri geometrici. Questo è aggiunto nel nome, come 3-etil-cis-2-eptano o 3-etil-trans-2-eptano.
Nomenclatura degli alchini
Per indovinare i nomi dei composti chimici che contengono legami tripli C≡C, il nome del composto è determinato dal numero di atomi di C nella catena più lunga.
Analogamente al caso degli alcheni, i nomi degli alchini indicano la posizione in cui si trova il triplo legame carbonio-carbonio; ad esempio, nei casi di HC≡C-CHDue-CH3, o "1-butino" e H3C-C≡C-CH3, o "2-butyne".
Proprietà
Gli idrocarburi insaturi comprendono un numero enorme di molecole diverse, motivo per cui presentano una serie di caratteristiche che li definiscono, che vengono identificate di seguito:
Doppi e tripli legami
I doppi e tripli legami di alcheni e alchini hanno caratteristiche speciali che li differenziano dai singoli legami: un singolo legame rappresenta il più debole dei tre, essendo formato da un legame sigma tra due molecole.
Il doppio legame è formato da un legame sigma e un pi greco, e il triplo legame da un legame sigma e due pi greco. Questo rende gli alcheni e gli alchini più forti e richiede più energia per abbattere quando si verificano le reazioni..
Inoltre, gli angoli di legame che si formano in un doppio legame sono 120º, mentre quelli del triplo legame sono 180º. Ciò significa che le molecole con tripli legami hanno un angolo lineare tra questi due atomi di carbonio..
Isomerizzazione cis-trans
Negli alcheni e in altri composti con doppi legami, si verifica un'isomerizzazione geometrica, che differisce sul lato dei legami in cui si trovano i gruppi funzionali che sono attaccati ai carboni coinvolti in questo doppio legame..
Quando i gruppi funzionali di un alchene sono orientati nella stessa direzione rispetto al doppio legame, questa molecola viene indicata come cis, ma quando i sostituenti sono in direzioni diverse, viene chiamata trans.
Questa isomerizzazione non è una semplice differenza di posizione; i composti possono variare notevolmente solo perché sono geometria cis o geometria trans.
I composti Cis di solito coinvolgono forze dipolo-dipolo (che hanno un valore netto di zero in trans); Inoltre, hanno una maggiore polarità, punti di ebollizione e fusione e hanno una densità maggiore rispetto alle loro controparti trans. Inoltre, i composti trans sono più stabili e rilasciano meno calore di combustione..
Acidità
Gli alcheni e gli alchini hanno un'acidità maggiore rispetto agli alcani, a causa della polarità dei loro doppi e tripli legami. Sono meno acidi degli alcoli e degli acidi carbossilici; e dei due, gli alchini sono più acidi degli alcheni.
Polarità
La polarità di alcheni e alchini è bassa, ancora di più nei composti trans alcheni, il che rende questi composti insolubili in acqua..
Tuttavia, gli idrocarburi insaturi si dissolvono facilmente in comuni solventi organici come eteri, benzene, tetracloruro di carbonio e altri composti a bassa o nessuna polarità..
Punti di ebollizione e di fusione
A causa della loro bassa polarità, i punti di ebollizione e di fusione degli idrocarburi insaturi sono bassi, quasi equivalenti a quelli degli alcani che hanno la stessa struttura di carbonio..
Anche così, gli alcheni hanno punti di ebollizione e di fusione inferiori rispetto ai corrispondenti alcani, potendo diminuire ancora di più se sono isomerici cis, come detto in precedenza..
Al contrario, gli alchini hanno punti di ebollizione e di fusione più elevati rispetto agli alcani e agli alcheni corrispondenti, sebbene la differenza sia solo di pochi gradi..
Infine, i cicloalcheni hanno anche temperature di fusione inferiori rispetto ai corrispondenti cicloalcani, a causa della rigidità del doppio legame..
Esempi
Etilene (CDueH4)
Un potente composto chimico grazie alla sua capacità di polimerizzazione, ossidazione e alogenazione, tra le altre caratteristiche.
Ethyne (C.DueHDue)
Chiamato anche acetilene, è un gas infiammabile che viene utilizzato come utile fonte di illuminazione e calore..
Propilene (C3H6)
Il secondo composto più utilizzato nell'industria chimica al mondo, è uno dei prodotti della termolisi del petrolio.
Ciclopentene (C5H8)
Un composto del tipo cicloalchene. Questa sostanza è usata come monomero per la sintesi di materie plastiche.
Articoli di interesse
Idrocarburi saturi o alcani.
Riferimenti
- Chang, R. (2007). Chimica, nona edizione. Messico: McGraw-Hill.
- Wikipedia. (s.f.). Alcheni. Estratto da en.wikipedia.org
- Boudreaux, K. A. (s.f.). Idrocarburi insaturi. Estratto da angelo.edu
- Tuckerman, M. E. (s.f.). Alcheni e alchini. Estratto da nyu.edu
- Università, L. T. (s.f.). Gli idrocarburi insaturi: alcheni e alchini. Estratto da chem.latech.edu


Nessun utente ha ancora commentato questo articolo.