
Eritroblasti cosa sono, eritropoiesi, patologie associate
Il eritroblasti sono cellule precursori degli eritrociti vertebrati. La diminuzione della concentrazione di ossigeno nei tessuti promuoverà eventi di differenziazione cellulare in queste cellule che daranno origine a eritrociti maturi. L'insieme di tutti questi eventi è noto come eritropoiesi.
Durante l'eritropoiesi, la sintesi dell'emoglobina aumenta. Una proteina abbondante negli eritrociti che media l'apporto di ossigeno ai tessuti e la disintossicazione dell'anidride carbonica dai tessuti, un prodotto di scarto tossico per le cellule della respirazione cellulare.
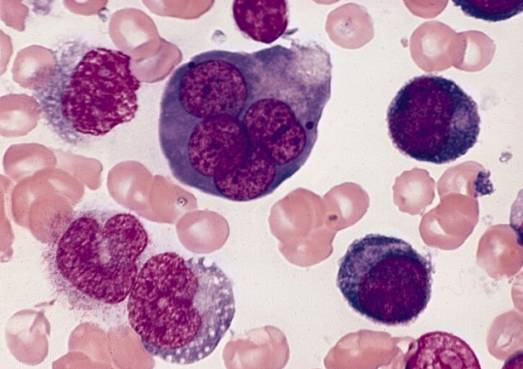
Gli errori nel processo di differenziazione degli eritroblasti danno origine a una serie di patologie del sangue che insieme vengono chiamate anemie megaloblastiche.
Indice articolo
- 1 Cosa sono gli eritrociti?
- 2 Cosa sono gli eritroblasti?
- 3 Cos'è l'eritropoiesi?
- 4 Differenziazione degli eritroblasti in eritrociti
- 5 Differenziazione cellulare
- 6 Patologie associate a errori nella differenziazione degli eritroblasti
- 7 Riferimenti
Cosa sono gli eritrociti?
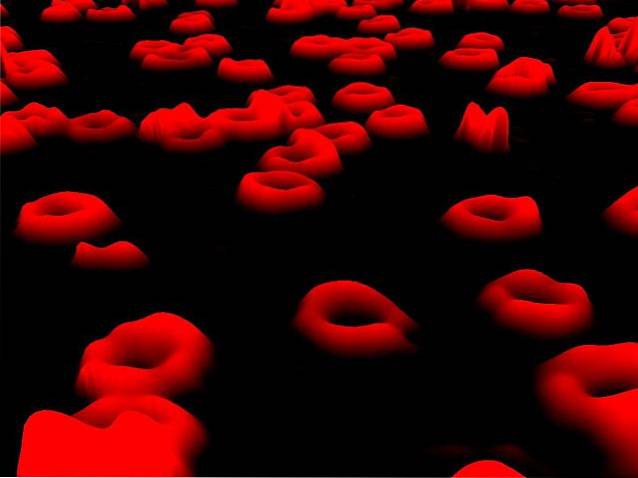
Hanno una morfologia caratteristica simile ai dischi biconcavi e la loro funzione principale è quella di effettuare il trasporto dell'ossigeno (O2) ai diversi tessuti del corpo, allo stesso tempo di disintossicarli dall'anidride carbonica (CO2) prodotta durante respirazione..
Questo scambio di CO2 per O2 è possibile perché queste cellule ospitano grandi quantità di una caratteristica proteina rossa chiamata emoglobina, in grado di interagire con entrambe le specie chimiche attraverso un gruppo eme presente nella loro struttura..
Una particolarità di queste cellule nei mammiferi rispetto al resto dei vertebrati è la mancanza di nucleo e di organelli citoplasmatici. Tuttavia, durante le fasi iniziali di produzione nelle prime fasi dello sviluppo embrionale, è stato osservato che i precursori cellulari da cui provengono presentano un nucleo transitorio.
Quest'ultimo non è sorprendente dato che le prime fasi dello sviluppo dell'embrione sono generalmente simili in tutti i vertebrati, divergendo solo le fasi che compromettono una maggiore differenziazione..
Cosa sono gli eritroblasti?
Gli eritroblasti sono cellule che daranno origine a eritrociti maturi dopo aver subito eventi consecutivi di differenziazione cellulare..
Queste cellule precursori provengono da un comune progenitore mieloide nel midollo osseo dei vertebrati come cellule nucleate, dotate di nuclei e organelli cellulari..
I cambiamenti nel contenuto del suo citoplasma e nella riorganizzazione del citoscheletro culmineranno nella generazione di eritrociti pronti per la circolazione. Questi cambiamenti rispondono a stimoli ambientali indicativi della diminuzione dell'ossigeno nei tessuti e quindi di una richiesta nella produzione di eritrociti..
Cos'è l'eritropoiesi?
Eritropoiesi è il termine utilizzato per definire il processo mediante il quale avviene la produzione e lo sviluppo dei globuli rossi, necessari per mantenere l'apporto di ossigeno ai diversi organi e tessuti..
Questo processo è finemente regolato dall'azione dell'eritropoietina (EPO), un ormone di sintesi renale che a sua volta è modulato dalle concentrazioni di ossigeno disponibili nei tessuti..
Basse concentrazioni di ossigeno nei tessuti inducono la sintesi di EPO da parte del fattore di trascrizione inducibile dall'ipossia (HIF-1), che stimola la proliferazione degli eritrociti legandosi ai recettori EpoR, presenti sulle cellule precursori degli eritrociti.
Nei mammiferi, l'eritropoiesi viene eseguita in due fasi chiamate eritropoiesi primitiva ed eritropoiesi definitiva..
Il primo si verifica nel sacco vitellino durante lo sviluppo embrionale, dando origine a grandi eritroblasti nucleati, mentre il secondo si verifica nel fegato fetale e continua nel midollo osseo dopo il secondo mese di gestazione, generando eritrociti enucleati più piccoli..
Altre proteine come la citochina antipoptotica Bcl-X, la cui trascrizione è regolata dal fattore di trascrizione GATA-1, influenzano positivamente anche il processo di eritropoiesi. Inoltre, sono necessari anche l'apporto di ferro, vitamina B12 e acido folico.
Differenziazione eritroblastica in eritrociti
Nel processo di eritropoiesi definitiva, gli eritrociti si formano nel midollo osseo da una cellula progenitrice indifferenziata o da un progenitore mieloide comune in grado di dare origine ad altre cellule come granulociti, monociti e piastrine..
Questa cellula deve ricevere i segnali extracellulari appropriati per compromettere la sua differenziazione verso la linea eritroide..
Una volta acquisito questo impegno, inizia una sequenza di eventi di differenziazione che inizia con la formazione del pronormoblasto, noto anche come proeritroblasto. Una grande cellula precursore degli eritroblasti con un nucleo.
Successivamente, il proeritroblasto sperimenterà una progressiva diminuzione del volume delle cellule nucleari accompagnata da un aumento della sintesi dell'emoglobina. Tutti questi cambiamenti avvengono lentamente mentre questa cellula attraversa diversi stadi cellulari: l'eritroblasto o normoblasto basofilo, l'eritroblasto policromatico e l'eritroblasto ortocromatico.
Il processo si conclude con la totale perdita del nucleo, nonché degli organelli presenti nell'eritroblasto ortocromatico, dando origine a un eritrocita maturo.
Per raggiungere finalmente questo, quest'ultimo deve passare attraverso lo stadio dei reticolociti, una cellula enucleata che contiene ancora organelli e ribosomi nel suo citoplasma. La rimozione completa del nucleo e degli organelli viene eseguita mediante esocitosi.
Gli eritrociti maturi lasciano il midollo osseo nel flusso sanguigno dove rimangono in circolazione per circa 120 giorni, prima di essere inghiottiti dai macrofagi. Pertanto, l'eritropoiesi è un processo che si verifica continuamente per tutta la vita di un organismo..
Differenziazione cellulare
Man mano che gli eritoblasti progrediscono verso la completa differenziazione in un eritrocita maturo, subiscono molteplici cambiamenti nel loro citoscheletro, nonché nell'espressione delle proteine di adesione cellulare..
I microfilamenti di actina depolimerizzano e viene assemblato un nuovo citoscheletro basato sulla spettrina. La spettrina è una proteina della membrana periferica situata sulla faccia citoplasmatica che interagisce con l'anchirina, una proteina che media il legame del citoscheletro con la proteina transmembrana della banda 3.
Questi cambiamenti nel citoscheletro e nell'espressione dei recettori Epo, così come i meccanismi che li modulano, sono fondamentali per la maturazione eritroide..
Ciò è dovuto al fatto che mediano l'instaurarsi di interazioni tra eritroblasti e cellule presenti nel microambiente del midollo osseo, facilitando la trasmissione dei segnali necessari per iniziare e terminare la differenziazione..
Una volta terminata la differenziazione, si verificano nuovi cambiamenti che favoriscono la perdita di adesione delle cellule al midollo e il loro rilascio nel flusso sanguigno dove svolgeranno la loro funzione..
Patologie associate a errori nella differenziazione degli eritroblasti
Errori durante la differenziazione degli eritroblasti nel midollo osseo danno luogo alla comparsa di patologie del sangue, come le anemie megaloblastiche. Questi derivano da carenze nell'apporto di vitamina B12 e folati necessari per promuovere la differenziazione degli eritroblasti..
Il termine megaloblastico si riferisce alle grandi dimensioni che gli eritroblasti e persino gli eritrociti raggiungono come prodotto dell'eritropoiesi inefficace caratterizzata da una sintesi del DNA difettosa.
Riferimenti
- Ferreira R, Ohneda K, Yamamoto M, Philipsen S. GATA1 function, un paradigma per i fattori di trascrizione nell'emopoiesi. Biologia molecolare e cellulare. 2005; 25 (4): 1215-1227.
- Kingsley PD, Malik J, Fantauzzo KA, Palis J. Eritroblasti primitivi derivati dal sacco vitellino enucleati durante l'embriogenesi dei mammiferi. Blood (2004); 104 (1): 19-25.
- Konstantinidis DG, Pushkaran S, Johnson JF, Cancelas JA, Manganaris S, Harris CE, Williams AE, Zheng Y, Kalfa TA. Segnalazione e requisiti citoscheletrici nell'enucleazione degli eritroblasti. Sangue. (2012); 119 (25): 6118-6127.
- Migliaccio AR. Enucleazione eritroblastica. Haematologica. 2010; 95: 1985-1988.
- Shivani Soni, Shashi Bala, Babette Gwynn, Kenneth E, Luanne L, Manjit Hanspal. L'assenza di proteina macrofagica eritroblastica (Emp) porta al fallimento dell'estrusione nucleare eritroblastica. Il giornale di chimica biologica. 2006; 281 (29): 20181-20189.
- Skutelsky E, Danon D. Uno studio al microscopio elettronico dell'eliminazione nucleare dal tardo eritroblasto. J Cell Biol, 1967; 33 (3): 625-635.
- Tordjman R, Delaire S, Plouet J, Ting S, Gaulard P, Fichelson S, Romeo P, Lemarchandel V. Gli eritroblasti sono una fonte di fattori angiogenici. Blood (2001); 97 (7): 1968-1974.



Nessun utente ha ancora commentato questo articolo.