
Caratteristiche dell'acido ipobromoso, struttura, usi

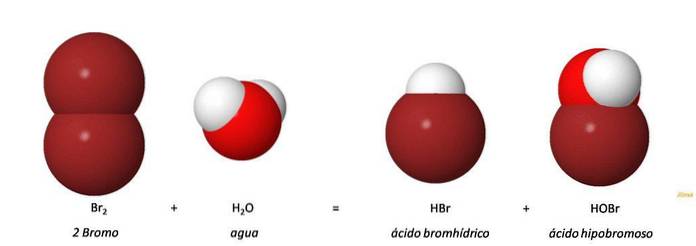
Il acido ipobromoso (HOBr, HBrO) è un acido inorganico prodotto dall'ossidazione dell'anione bromuro (Br-). L'aggiunta di bromo all'acqua dà acido bromidrico (HBr) e acido ipobromoso (HOBr) attraverso una reazione di sproporzione. Br2 + H2O = HOBr + HBr
L'acido ipobromoso è un acido molto debole, alquanto instabile, esistente come soluzione diluita a temperatura ambiente. È prodotto negli organismi vertebrati a sangue caldo (compreso l'uomo), dall'azione dell'enzima eosinofilo perossidasi.
La scoperta che l'acido ipobromoso può regolare l'attività del collagene IV ha attirato molta attenzione..
Indice articolo
- 1 Struttura
- 1.1 2D
- 1.2 3D
- 2 Proprietà fisiche e chimiche
- 3 usi
- 4 Interazioni biomolecolari
- 5 Riferimenti
Struttura
2D
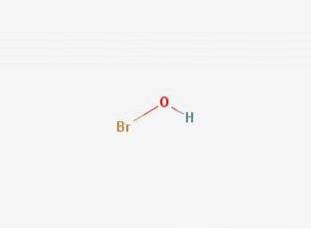
3D

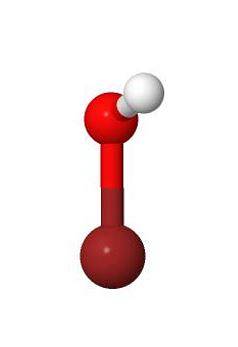
Proprietà fisiche e chimiche
- Aspetto solidi gialli: solidi gialli.
- Aspetto: solido giallo.
- Peso molecolare: 96,911 g / mol.
- Punto di ebollizione: 20-25 ° C.
- Densità: 2.470 g / cm3.
- Acidità (pKa): 8,65.
- Le proprietà chimiche e fisiche dell'acido ipobromoso sono simili a quelle di altri ipoaliti..
- Si presenta come una soluzione diluita a temperatura ambiente.
- I solidi ipobromiti sono di colore giallo e hanno un odore aromatico particolare.
- È un potente battericida e disinfettante per l'acqua.
- Ha un pKa di 8,65 e si dissocia parzialmente in acqua a pH 7.
Applicazioni
- L'acido ipobromoso (HOBr) è usato come agente sbiancante, ossidante, deodorante e disinfettante, grazie alla sua capacità di uccidere le cellule di molti patogeni.
- Viene utilizzato dall'industria tessile come agente sbiancante ed essiccante.
- Utilizzato anche in vasche idromassaggio e spa come agente germicida.
Interazioni biomolecolari
Il bromo è onnipresente negli animali come il bromuro ionico (Br-), ma fino a tempi recenti la sua funzione essenziale era sconosciuta..
Recenti ricerche hanno dimostrato che il bromo è essenziale per l'architettura della membrana basale e lo sviluppo dei tessuti.
L'enzima perossidina utilizza HOBr per reticolare la sulfilimina, che è reticolata negli scaffold di collagene IV della membrana basale..
L'acido ipobromoso è prodotto negli organismi vertebrati a sangue caldo dall'azione dell'enzima eosinofilo perossidasi (EPO).
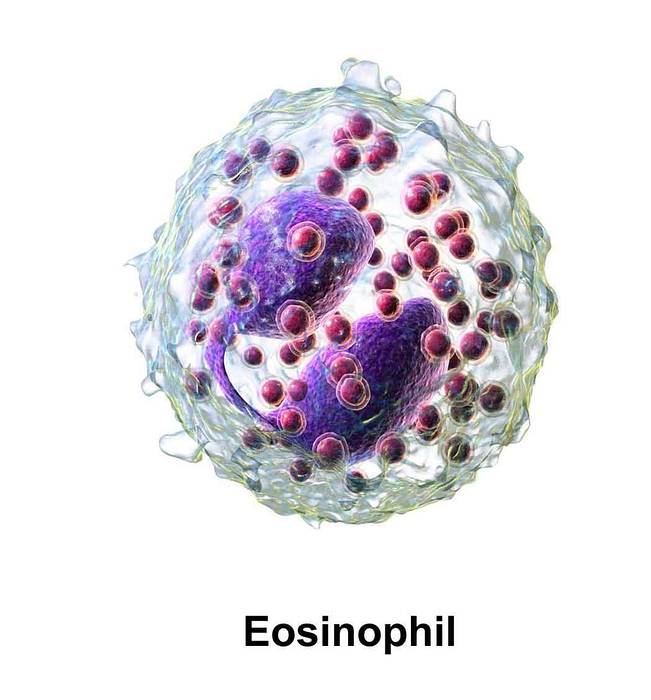
L'EPO genera HOBr da H2O2 e Br- in presenza di una concentrazione plasmatica di Cl-.
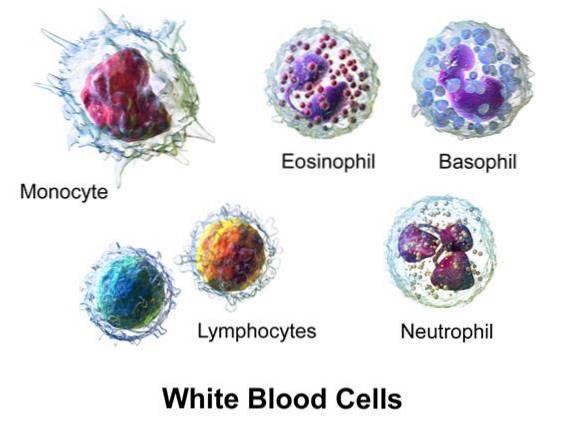
La mieloperossidasi (MPO), da monociti e neutrofili, genera acido ipocloroso (HOCl) da H2O2 e Cl-.
EPO e MPO svolgono un ruolo importante nei meccanismi di difesa dell'ospite contro i patogeni, utilizzando rispettivamente HOBr e HOCl.
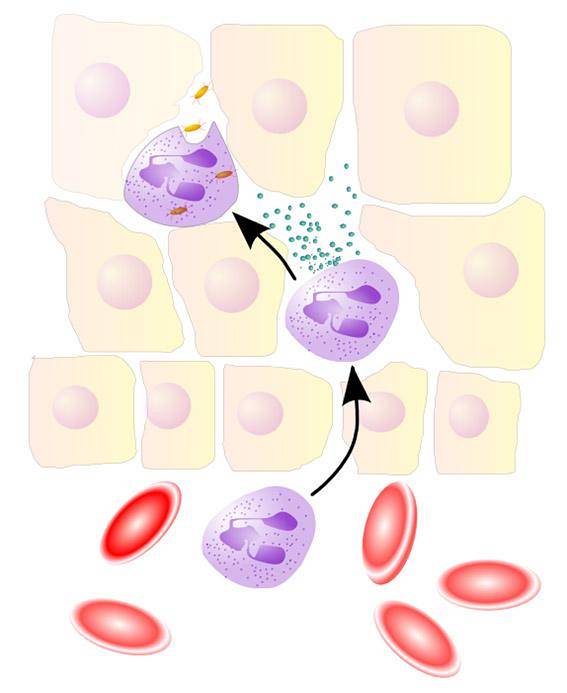
Il sistema MPO / H2O2 / Cl- in presenza di Br- genera anche HOBr facendo reagire l'HOCl formato con Br-. Più che un potente ossidante, HOBr è un potente elettrofilo.
La concentrazione plasmatica di Br- è più di 1000 volte inferiore a quella dell'anione cloruro (Cl-). Di conseguenza, anche la produzione endogena di HOBr è inferiore rispetto a HOCl.
Tuttavia, HOBr è significativamente più reattivo di HOCl quando l'ossidabilità dei composti studiati non è rilevante, quindi la reattività di HOBr potrebbe essere più associata alla sua forza elettrofila che al suo potere ossidante (Ximenes, Morgon & de Souza, 2015).
Sebbene il suo potenziale redox sia inferiore a quello di HOCl, HOBr reagisce con gli amminoacidi più velocemente di HOCl.
L'alogenazione dell'anello di tirosina di HOBr è 5000 volte più veloce di quella di HOCl.
HOBr reagisce anche con le basi azotate nucleosidiche e il DNA.
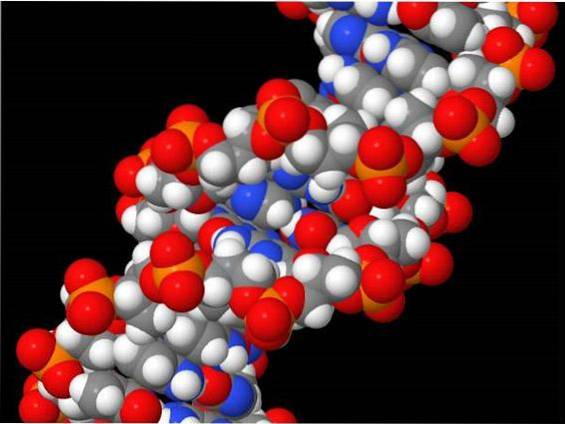
2'-desossicitidina, adenina e guanina, generano 5-bromo-2'-deossicitidina, 8-bromoadenina e 8-bromoguanina nei sistemi EPO / H2O2 / Br- e MPO / H2O2 / Cl- / Br- (Suzuki, Kitabatake e Koide , 2016).
McCall, et al. (2014) hanno dimostrato che Br è un cofattore necessario per la formazione di legami crociati sulfilimminici catalizzati dall'enzima perossidasina, una modifica post-traduzionale essenziale per l'architettura del collagene IV delle membrane basali e lo sviluppo dei tessuti..
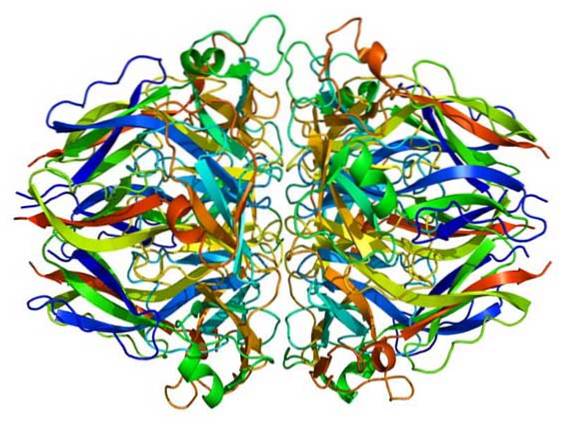
Le membrane basali sono matrici extracellulari specializzate che sono mediatori chiave della trasduzione del segnale e del supporto meccanico delle cellule epiteliali..
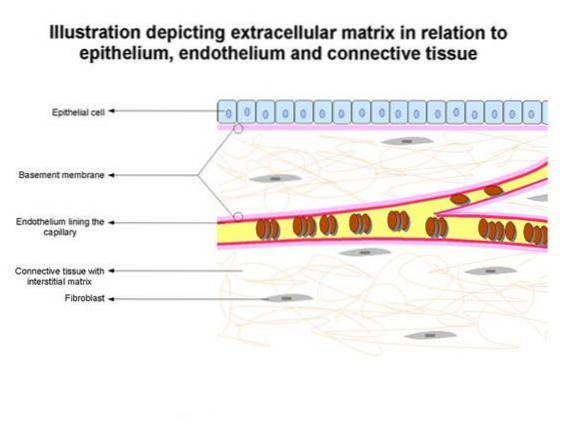
Le membrane basali definiscono l'architettura del tessuto epiteliale e facilitano la riparazione dei tessuti dopo la lesione, tra le altre funzioni..
Incorporato all'interno della membrana basale è uno scaffold di collagene IV reticolato con sulfilimine, che conferisce la funzionalità della matrice nei tessuti multicellulari di tutti gli animali..
Gli scaffold di collagene IV forniscono resistenza meccanica, fungono da ligando per integrine e altri recettori della superficie cellulare e interagiscono con i fattori di crescita per stabilire gradienti di segnalazione..
La sulfilimina (solfimmide) è un composto chimico che contiene un doppio legame zolfo-azoto. I legami sulfilimminici stabilizzano i filamenti di collagene IV presenti nella matrice extracellulare.
Questi legami collegano covalentemente i residui di metionina 93 (Met93) e idrossilisina 211 (Hyl211) di filamenti polipeptidici adiacenti per formare un trimero di collagene più grande..
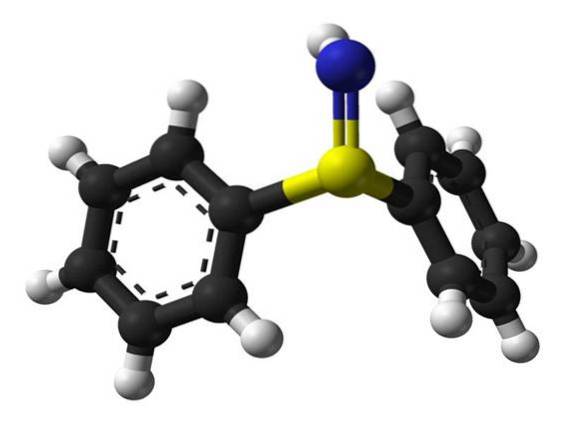
La perossidina forma acido ipobromoso (HOBr) e acido ipocloroso (HOCl) da bromuro e cloruro, rispettivamente, che possono mediare la formazione di legami crociati sulfilimminici..
Il bromuro, convertito in acido ipobromoso, forma un intermedio dello ione bromosolfonio (S-Br) che partecipa alla formazione dei legami crociati.
McCall, et al. (2014) hanno dimostrato che la carenza alimentare di Br è letale nella mosca Drosophila, mentre la sostituzione di Br ne ripristina la vitalità.
Hanno anche stabilito che il bromo è un oligoelemento essenziale per tutti gli animali a causa del suo ruolo nella formazione dei legami sulfilimminici e del collagene IV, che è di vitale importanza per la formazione delle membrane basali e lo sviluppo dei tessuti..
Riferimenti
- ChemIDplus, (2017). Struttura 3D di 13517-11-8 - Acido ipobromoso [immagine] Estratto da nih.gov.
- ChemIDplus, (2017). Struttura 3D di 60-18-4 - Tirosina [USAN: INN] [immagine] Estratto da nih.gov.
- ChemIDplus, (2017). Struttura 3D di 7726-95-6 - Bromo [immagine] Estratto da nih.gov.
- ChemIDplus, (2017). Struttura 3D di 7732-18-5 - Acqua [immagine] Recuperato da nih.gov.
- Emw, (2009). Proteina COL4A1 PDB 1li1 [immagine] Recuperato da wikipedia.org.
- Mills, B. (2009). Diphenylsulfimide-from-xtal-2002-3D-balls [immagine] Recuperato da wikipedia.org.
- PubChem, (2016). Acido ipobromoso [immagine] Estratto da nih.gov.
- Steane, R. (2014). The DNA Molecule - ruotabile in 3 dimensioni [immagine] Recuperato da biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [immagine] Recuperato da wikipedia.org.



Nessun utente ha ancora commentato questo articolo.