
Caratteristiche, formazione, tipi ed esempi dei biofilm
Il biofilm o biofilm Sono comunità di microrganismi attaccati a una superficie, che vivono in una matrice autogenerata di sostanze polimeriche extracellulari. Furono inizialmente descritti da Antoine von Leeuwenhoek, quando esaminò gli "animaletti" (da lui così chiamati), su un piatto di materiale dai suoi stessi denti nel XVII secolo..
La teoria che concettualizza i biofilm e descrive il loro processo di formazione non è stata sviluppata fino al 1978. Si è scoperto che la capacità dei microrganismi di formare biofilm sembra essere universale..
I biofilm possono esistere in ambienti diversi come sistemi naturali, acquedotti, serbatoi di stoccaggio dell'acqua, sistemi industriali, nonché in un'ampia varietà di mezzi come dispositivi medici e dispositivi per la permanenza in pazienti ospedalieri (come cateteri, per esempio).
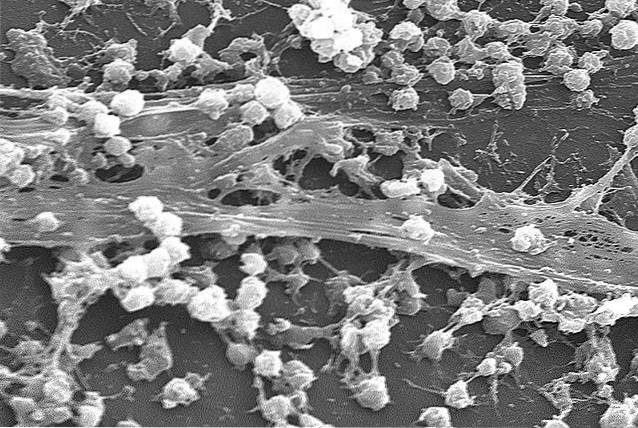
Attraverso l'uso della microscopia elettronica a scansione e della microscopia laser a scansione confocale, è stato scoperto che i biofilm non sono depositi omogenei e non strutturati di cellule e limo accumulato, ma piuttosto complesse strutture eterogenee..
I biofilm sono comunità complesse di cellule associate su una superficie, racchiuse in una matrice polimerica altamente idratata la cui acqua circola attraverso i canali aperti della struttura..
Molti organismi che hanno avuto successo nella loro sopravvivenza di milioni di anni nell'ambiente, ad esempio le specie dei generi Pseudomonas Y Legionella, utilizzare la strategia del biofilm in ambienti diversi dai loro ambienti nativi nativi.
Indice articolo
- 1 Caratteristiche dei biofilm
- 1.1 Caratteristiche chimiche e fisiche della matrice del biofilm
- 1.2 Caratteristiche ecofisiologiche dei biofilm
- 2 Formazione di biofilm
- 2.1 Adesione iniziale alla superficie
- 2.2 Formazione di un monostrato e microcolonie in multistrato
- 2.3 Produzione della matrice extracellulare polimerica e maturazione del biofilm tridimensionale
- 3 tipi di biofilm
- 3.1 Numero di specie
- 3.2 Ambiente di formazione
- 3.3 Tipo di interfaccia in cui vengono generati
- 4 Esempi di biofilm
- 4.1 -Placca dentale
- 4.2 -Biofilm in acque nere
- 4.3 - biofilm subaereo
- 4.4 -Biofilm di agenti causali di malattie umane
- 4.5-Peste bubbonica
- 4.6 -Cateteri venosi ospedalieri
- 4.7 -Nel settore
- 5 Resistenza dei biofilm a disinfettanti, germicidi e antibiotici
- 6 Riferimenti
Caratteristiche del biofilm
Caratteristiche chimiche e fisiche della matrice del biofilm
-Le sostanze polimeriche extracellulari secrete da microrganismi del biofilm, macromolecole polisaccaridiche, proteine, acidi nucleici, lipidi e altri biopolimeri, per lo più molecole altamente idrofile, si incrociano per formare una struttura tridimensionale chiamata matrice del biofilm..
-La struttura della matrice è altamente viscoelastica, ha proprietà di gomma, è resistente alla trazione e alla rottura meccanica.
-La matrice ha la capacità di aderire alle superfici dell'interfaccia, inclusi gli spazi interni dei mezzi porosi, attraverso polisaccaridi extracellulari che agiscono come gengive aderenti..
-La matrice polimerica è prevalentemente anionica e include anche sostanze inorganiche come i cationi metallici..
-Dispone di canali d'acqua attraverso i quali circolano ossigeno, nutrienti e sostanze di scarto che possono essere riciclati..
-Questa matrice del biofilm funziona come mezzo di protezione e sopravvivenza contro ambienti avversi, una barriera contro gli invasori fagocitici e contro l'ingresso e la diffusione di disinfettanti e antibiotici..
Caratteristiche ecofisiologiche dei biofilm
-La formazione della matrice in gradienti disomogenei produce una varietà di microhabitat, che consente alla biodiversità di esistere all'interno del biofilm..
-All'interno della matrice, la forma di vita cellulare è radicalmente diversa dalla vita libera e non associata. I microrganismi del biofilm sono immobilizzati, molto vicini tra loro, associati in colonie; questo fatto consente che si verifichino interazioni intense.
-Le interazioni tra i microrganismi nel biofilm includono la comunicazione attraverso segnali chimici in un codice chiamato "quorum sensing"..
-Esistono altre importanti interazioni come il trasferimento genico e la formazione di micro-consorzi sinergici..
-Il fenotipo del biofilm può essere descritto in termini di geni espressi dalle cellule associate. Questo fenotipo è alterato rispetto al tasso di crescita e alla trascrizione genica.
-Gli organismi all'interno del biofilm possono trascrivere geni che non trascrivono le loro forme di vita planctoniche o libere.
-Il processo di formazione del biofilm è regolato da geni specifici, trascritti durante l'adesione cellulare iniziale.
-Nello spazio ristretto della matrice ci sono meccanismi di cooperazione e competizione. La competizione genera un adattamento costante nelle popolazioni biologiche.
-Viene generato un sistema digestivo esterno collettivo, che trattiene gli enzimi extracellulari vicino alle cellule.
-Questo sistema enzimatico permette di sequestrare, accumulare e metabolizzare nutrienti disciolti, colloidali e / o sospesi.
-La matrice funziona come un'area di riciclaggio esterna comune, un magazzino per i componenti delle cellule lisate, che funge anche da archivio genetico collettivo..
-Il biofilm funge da barriera strutturale protettiva contro i cambiamenti ambientali come l'essiccazione, l'azione di biocidi, antibiotici, risposte immunitarie dell'ospite, agenti ossidanti, cationi metallici, radiazioni ultraviolette ed è anche una difesa contro molti predatori come i protozoi fagocitici e gli insetti..
-La matrice del biofilm costituisce un ambiente ecologico unico per i microrganismi, consentendo uno stile di vita dinamico per la comunità biologica. I biofilm sono veri microecosistemi.
Formazione di biofilm
La formazione del biofilm è un processo in cui i microrganismi passano da uno stato nomade unicellulare a vita libera a uno stato sedentario multicellulare, dove la crescita successiva produce comunità strutturate con differenziazione cellulare.
Lo sviluppo del biofilm avviene in risposta a segnali ambientali extracellulari e segnali auto-generati.
I ricercatori che hanno studiato i biofilm concordano sul fatto che è possibile costruire un modello ipotetico generalizzato per spiegare la loro formazione.
Questo modello di formazione del biofilm si compone di 5 fasi:
- Adesione iniziale alla superficie.
- Formazione di un monostrato.
- Migrazione per formare microcolonie multistrato.
- Produzione della matrice extracellulare polimerica.
- Maturazione del biofilm tridimensionale.

Adesione iniziale alla superficie
La formazione del biofilm inizia con l'adesione iniziale dei microrganismi alla superficie solida, dove vengono immobilizzati. È stato scoperto che i microrganismi hanno sensori di superficie e che le proteine di superficie sono coinvolte nella formazione della matrice.
Negli organismi non mobili, quando le condizioni ambientali sono favorevoli, aumenta la produzione di adesine sulla loro superficie esterna. In questo modo, aumenta la sua capacità di adesione cellula-cellula e superficie cellulare..
Nel caso delle specie mobili, i singoli microrganismi si trovano su una superficie e questo è il punto di partenza verso un cambiamento radicale nel loro modo di vivere da nomade mobile libero, a sedentario, quasi sessile.
La capacità di movimento si perde perché alla formazione della matrice partecipano diverse strutture come flagelli, ciglia, pilus e fimbria, oltre alle sostanze adesive.
Quindi, in entrambi i casi (microrganismi mobili e non mobili), si formano piccoli aggregati o microcolonie e si genera un contatto cellula-cellula più intenso; cambiamenti fenotipici adattivi al nuovo ambiente si verificano nelle cellule raggruppate.
Formazione di un monostrato e microcolonie in multistrato
Inizia la produzione di sostanze polimeriche extracellulari, avviene la formazione iniziale in monostrato e il successivo sviluppo in multistrato.
Produzione della matrice extracellulare polimerica e maturazione del biofilm tridimensionale
Infine, il biofilm raggiunge il suo stadio di maturità, con un'architettura tridimensionale e la presenza di canali attraverso i quali circolano acqua, nutrienti, sostanze chimiche di comunicazione e acidi nucleici..
La matrice del biofilm trattiene le cellule e le tiene unite, favorendo un alto grado di interazione con la comunicazione intercellulare e la formazione di consorzi sinergici. Le cellule del biofilm non sono completamente immobilizzate, possono muoversi al suo interno e anche staccarsi.
Tipi di biofilm
Numero di specie
In base al numero di specie che partecipano al biofilm, quest'ultimo può essere classificato in:
- Biofilm di una specie. Ad esempio, biofilm costituiti da Streptococcus mutans o Vellionella parvula.
- Biofilm di due specie. Ad esempio, l'associazione di Streptococcus mutans Y Vellionella parvula nei biofilm.
- Biofilm polimicrobici, composti da molte specie. Ad esempio, placca dentale.
Ambiente di formazione
Inoltre, a seconda dell'ambiente in cui si formano, i biofilm possono essere:
- Naturale
- Industriale
- Domestico
- Ospitale

Tipo di interfaccia in cui vengono generati
D'altra parte, a seconda del tipo di interfaccia in cui sono formati, è possibile classificarli in:
- Biofilm dell'interfaccia solido-liquido, come quelli formati in acquedotti e serbatoi, tubazioni e serbatoi d'acqua in genere.
- Biofilm interfaccia solido-gas (SAB per il suo acronimo in inglese Sub Aereal Biofilms); che sono comunità microbiche che si sviluppano su superfici minerali solide, direttamente esposte all'atmosfera e alla radiazione solare. Si trovano in edifici, rocce nude del deserto, montagne, tra gli altri.
Esempi di biofilm
-Placca dentale
La placca dentale è stata studiata come un interessante esempio di una comunità complessa che vive nei biofilm. I biofilm delle placche dentali sono duri e non elastici, per la presenza di sali inorganici, che conferiscono rigidità alla matrice polimerica..
I microrganismi della placca dentale sono molto vari e ci sono tra 200 e 300 specie associate nel biofilm.
Tra questi microrganismi ci sono:
- Il genere Streptococco; costituito da batteri acidurici che demineralizzano lo smalto e la dentina e danno inizio alla carie dentale. Ad esempio, la specie: mutans, S. sobrinus, S. sanguis, S. salivalis, S. mitis, S. oralis Y S. milleri.
- Il genere Lactobacillus, costituito da batteri acidofili che denaturano le proteine della dentina. Ad esempio, la specie: casei, L. fermentum, L. acidophillus.
- Il genere Actinomyces, che sono microrganismi acidurici e proteolitici. Tra questi, le specie: viscosus, A. odontoliticus Y A. naeslundii.
- E altri generi, Che cosa: Candida albicans, Bacteroides forsythus, Porphyromonas gingivalis Y Actinobacillus actinomycetecomitans.
-Biofilm nelle acque reflue
Un altro esempio interessante sono le acque reflue domestiche, dove vivono in biofilm attaccati a tubi, microrganismi nitrificanti che ossidano ammonio, nitriti e batteri nitrificanti autotrofi..
Tra i batteri ossidanti l'ammonio di questi biofilm, le specie numericamente dominanti sono quelle del genere Nitrosomonas, distribuito in tutta la matrice del biofilm.
I componenti maggioritari all'interno del gruppo degli ossidanti nitriti sono quelli del genere Nitrospira, che si trovano solo nella parte interna del biofilm.
-Biofilm subaerici
I biofilm subaerie sono caratterizzati da una crescita irregolare su superfici minerali solide come rocce ed edifici urbani. Questi biofilm presentano associazioni dominanti di funghi, alghe, cianobatteri, batteri eterotrofi, protozoi e animali microscopici..
In particolare, i biofilm SAB possiedono microrganismi chemolitotrofici, in grado di utilizzare sostanze chimiche minerali inorganiche come fonti di energia..
I microrganismi chemolitotrofici hanno la capacità di ossidare composti inorganici come H.Due, NH3, NONDue, S, HS, FeDue+ e sfruttare l'energia del potenziale prodotto elettrico delle ossidazioni nel loro metabolismo.
Tra le specie microbiche presenti nei biofilm subaerei ci sono:
- Batteri del genere Geodermatophilus; cianobatteri del genere Chrococcoccidiopsis, specie coccoide e filamentose come Calothrix, Gloeocapsa, Nostoc, Stigonema, Phormidium,
- Alghe verdi dei generi Chlorella, Desmococcus, Phycopeltis, Printzina, Trebouxia, Trentepohlia e Stichococcus.
- Batteri eterotrofi (dominanti nei biofilm subaerei): Arthrobacter sp., Bacillus sp., Micrococcus sp., Paenibacillus sp., Pseudomonas sp. e Rhodococcus sp.
- Batteri chemioorganotrofici e funghi come Actynomycetales (streptomiceti e Geodermatophilaceae), Proteobatteri, Actinobacteria, Acidobacteria e Bacteroides-Cytophaga-Flavobacterium.
-Biofilm di agenti causali di malattie umane
Molti dei batteri noti come agenti causali delle malattie umane vivono nei biofilm. Tra questi ci sono: Vibrio cholerae, Vibrio parahaemolyticus, Vibrio fischeri, Vellionella parvula, Streptococcus mutans Y Legionella pneumophyla.
-Piaga bubbonica
Interessante è la trasmissione della peste bubbonica tramite il morso delle pulci, un adattamento relativamente recente dell'agente batterico che causa questa malattia., Yersinia pestis.
Questo batterio cresce come un biofilm attaccato al tratto digerente superiore del vettore (la pulce). Durante un morso, la pulce rigurgita il biofilm che lo contiene Yersinia pestis nel derma e quindi inizia l'infezione.
-Cateteri venosi ospedalieri
I microrganismi isolati dal biofilm sui cateteri venosi centrali espiantati includono una serie sorprendente di batteri Gram-positivi e Gram-negativi, così come altri microrganismi..
Diversi studi scientifici riportano come batteri Gram-positivi da biofilm nei cateteri venosi: Corynebacterium spp., Enterococcus sp., Enterococcus faecalis, Enterococcus faecium, Staphylococcus spp., Stafilococco aureola, Staphylococcus epidermidis, Streptococco spp. Y Streptococcus pneumoniae.
Tra i batteri Gram-negativi isolati da questi biofilm, si riportano i seguenti: Acinetobacter spp., Acinetobacter calcoaceticus, Acinetobacter anitratus, Enterobacter cloacae, Enterobacter aerogens, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Pseudomonas aeruginosa, Pseudomonas putida, Proteus spp., Providencia spp. Y Serratia marcescens.
Altri organismi presenti in questi biofilm sono: Candida spp., Candida albicans, Candida tropicalis Y Mycobacterium chelonei.
-Nell'industria
Per quanto riguarda il funzionamento dell'industria, i biofilm generano ostruzioni nei tubi, danni alle apparecchiature, interferenze in processi come i trasferimenti di calore quando si coprono le superfici degli scambiatori o la corrosione delle parti metalliche..
Industria alimentare
La formazione di film nell'industria alimentare può generare significativi problemi operativi e di salute pubblica.
Gli agenti patogeni associati nei biofilm possono contaminare i prodotti alimentari con batteri patogeni e causare gravi problemi di salute pubblica ai consumatori.
Tra i biofilm di patogeni associati all'industria alimentare ci sono:
Listeria monocytogenes
Questo agente patogeno utilizza nella fase iniziale della formazione del biofilm, flagelli e proteine di membrana. Forma biofilm sulle superfici in acciaio delle affettatrici.
Nell'industria lattiero-casearia, i biofilm di Listeria monocytogenes nel latte liquido e nei prodotti derivati dal latte. I residui di latticini in tubi, serbatoi, contenitori e altri dispositivi favoriscono lo sviluppo di biofilm di questo patogeno che li utilizza come nutrienti disponibili..
Pseudomonas spp.
I biofilm di questi batteri possono essere trovati nelle strutture dell'industria alimentare, come pavimenti, scarichi e sulle superfici di alimenti come carne, verdura e frutta, nonché derivati a bassa acidità del latte.
Pseudomonas aeruginosa secerne varie sostanze extracellulari che vengono utilizzate nella formazione della matrice polimerica del biofilm, aderendo a un gran numero di materiali inorganici come l'acciaio inossidabile.
Pseudomonas possono coesistere all'interno del biofilm in associazione con altri batteri patogeni come Salmonella Y Listeria.
Salmonella spp.
Le specie di Salmonella sono il primo agente causale di zoonosi di eziologia batterica e focolai di tossinfezione alimentare.
Studi scientifici lo hanno dimostrato Salmonella possono aderire come biofilm a superfici in calcestruzzo, acciaio e plastica negli impianti di lavorazione degli alimenti.
Le specie di Salmonella hanno strutture superficiali con proprietà aderenti. Inoltre, produce cellulosa come sostanza extracellulare, che è il componente principale della matrice polimerica..
Escherichia coli
Utilizza flagelli e proteine di membrana nella fase iniziale della formazione del biofilm. Produce anche cellulosa extracellulare per generare il reticolo tridimensionale della matrice nel biofilm..
Resistenza dei biofilm a disinfettanti, germicidi e antibiotici
I biofilm offrono protezione ai microrganismi che li compongono, all'azione di disinfettanti, germicidi e antibiotici. I meccanismi che consentono questa funzionalità sono i seguenti:
- Penetrazione ritardata dell'agente antimicrobico attraverso la matrice tridimensionale del biofilm, a causa della diffusione molto lenta e della difficoltà nel raggiungere la concentrazione effettiva.
- Tasso di crescita alterato e basso metabolismo dei microrganismi nel biofilm.
- Cambiamenti nelle risposte fisiologiche dei microrganismi durante la crescita del biofilm, con espressione genica di resistenza alterata.
Riferimenti
- Biofilm batterici. (2008). Argomenti attuali in microbiologia e immunologia. Tony Romeo Editor. Vol. 322 Berlino, Hannover: Springer Verlag. pp301.
- Donlan, R.M. e Costerton, J.W. (2002). Biofilm: meccanismi di sopravvivenza di microrganismi clinicamente rilevanti. Revisioni cliniche di microbiologia.15 (2): 167-193. doi: 10.1128 / CMR.15.2.167-193.2002
- Fleming, H.C. e Wingender, F. (2010). La matrice del biofilm. Nature Reviews Microbiology. 8: 623-633.
- Gorbushina, A. (2007). La vita sulle rocce. Microbiologia ambientale. 9 (7): 1-24. doi: 10.1111 / j.1462-2920.2007.01301.x
- O'Toole, G., Kaplan, H.B. e Kolter, R. (2000). Formazione di biofilm come sviluppo microbico. Revisione annuale di microbiologia. 54: 49-79. doi: 1146 / annurev.microbiol.54.1.49
- Hall-Stoodley, L., Costerton, J.W. e Stoodley, P. (2004). Biofilm batterici: dall'ambiente naturale alle malattie infettive. Nature Reviews Microbiology. 2: 95-108.
- Whitchurch, C.B., Tolker-Nielsen, T., Ragas, P. e Mattick, J. (2002). DNA extracellulare necessario per la formazione del biofilm batterico. 259 (5559): 1487-1499. doi: 10.1126 / science.295.5559.1487



Nessun utente ha ancora commentato questo articolo.