
Acinetobacter baumannii caratteristiche, morfologia, sintomi
Acinetobacter baumannii È un batterio gram-negativo, appartenente all'ordine degli Pseudomonas. Nel corso della sua storia tassonomica è stato localizzato nei generi Micrococcus, Moraxella, Alcaligenes, Mirococcuscalco-aceticus, Herellea Y Achromobacter, fino a quando non è stato inserito nel suo genere attuale nel 1968.
PER. baumannii è un batterio patogeno, considerato la specie più frequentemente implicata nelle infezioni del suo genere. È stato identificato come coinvolto in vari tipi di infezioni come setticemia, polmonite e meningite.
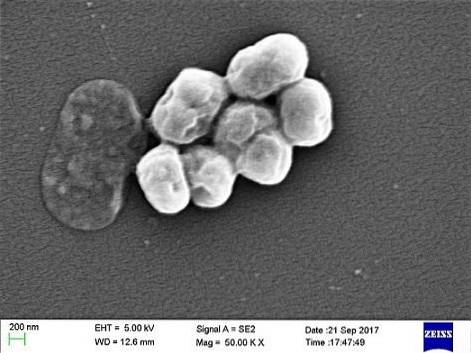
È un parassita opportunista che ha un'incidenza significativa nelle malattie ospedaliere o nosocomiali. La trasmissione per ventilazione meccanica è stata identificata come un'importante causa di contagio, soprattutto nelle Unità di Terapia Intensiva.
Nonostante sia considerato un patogeno di basso grado, ha la capacità di aumentare la sua virulenza nei ceppi coinvolti in frequenti infezioni. Ha una grande capacità di sviluppare resistenza e multi-resistenza agli antibiotici.
Negli ospedali è trasmesso principalmente dal contatto del personale, dall'uso di materiali ospedalieri contaminati e anche attraverso l'aria su brevi distanze.
L'Organizzazione mondiale della sanità include A. baumannii su un elenco di patogeni resistenti per i quali sono urgentemente necessari nuovi antibiotici, assegnandogli la categoria 1, con priorità critica.
Indice articolo
- 1 Caratteristiche di Acinetobacter baumannii
- 2 Morfologia
- 3 Metabolismo
- 4 Resistenza agli antibiotici
- 5 patologie
- 6 sintomi
- 7 Trattamento
- 8 Riferimenti
Caratteristiche di Acinetobacter baumannii
Tutte le specie del genere Acinetobacter hanno un'ampia distribuzione in diverse nicchie naturali. A. baumannii può abitare naturalmente la pelle di persone sane, potendo colonizzare le superfici mucose, che costituisce un importante serbatoio epidemiologico. Tuttavia, l'habitat di A. baumannii è quasi esclusivo per le impostazioni ospedaliere.
Questi batteri sono privi di flagelli o strutture utilizzate per la locomozione. Tuttavia, raggiungono il movimento attraverso strutture che consentono loro di estendersi e ritrarsi e attraverso meccanismi chimici come l'escrezione di un film di un esopolisaccaride ad alto peso molecolare dietro i batteri..
A. baumannii può colonizzare un gran numero di ambienti viventi o inerti e ha una grande capacità di sopravvivere su superfici artificiali per un periodo di tempo prolungato.
Questa capacità è probabilmente dovuta alla loro capacità di resistere alla disidratazione, di utilizzare varie fonti di carbonio attraverso varie vie metaboliche e per la capacità di formare biofilm. Per questo motivo è comune trovarlo in materiale ospedaliero, come cateteri e dispositivi di ventilazione meccanica..
Morfologia
A. baumannii è un coccobacillus, di forma intermedia tra cocchi e bastoncelli. Misurano da 1,5 a 2,5 da 1 a 1,5 micron quando le popolazioni sono in una fase logaritmica di crescita. Sono più sferiche quando raggiungono la fase stazionaria.
Metabolismo
I batteri A. baumannii non è un fermentatore di glucosio; è rigorosamente aerobico, cioè richiede ossigeno per il suo metabolismo.
Le specie del genere Acinetobacter sono le uniche della famiglia delle Moraxellaceae prive di citocromo c ossidasi, per le quali danno risultati negativi nei test ossidasi.
A. baumannii cresce a temperature che variano tra 20 e 44ºC, essendo la sua temperatura ottimale tra 30 e 35ºC.
Resistenza agli antibiotici
La costante generazione di resistenza agli antibiotici non solo ostacola il trattamento e il controllo delle infezioni causate da A. baumannii, promuove inoltre la selezione di ceppi multiresistenti endemici ed epidemici.
Alcuni meccanismi intrinseci di A. baumannii, che promuovono la resistenza agli antibiotici:
- La presenza di Le β-lattamasi conferiscono resistenza ai b-lattamici.
- La produzione di enzimi specifici come l'ammoniglucoside-3'-fosfotransferasi VI, inattiva l'amikacina.
- La presenza di oxacillinase OXA-51 idrolizza penicilline e carbapenemi.
- La presenza e la sovraespressione delle pompe a reflusso, che sono pompe che espellono dalla cellula piccole molecole che riescono a penetrare nel citoplasma, riducendo così la loro suscettibilità agli antibiotici.
I biofilm generati da A. baumannii alterare il metabolismo dei microrganismi, riducendo la loro sensibilità agli antibiotici, oltre a fornire una barriera fisica contro le grandi molecole e prevenire la disidratazione dei batteri.
Patologie
A. baumannii colonizza un nuovo ospite tramite il contatto con persone infette o con apparecchiature mediche contaminate. Prima di tutto, questo batterio si attacca alla pelle e alle superfici delle mucose. Per riprodursi, deve sopravvivere agli antibiotici e agli inibitori e alle condizioni di queste superfici..
L'aumento del numero di batteri sulle superfici mucose, in particolare in condizioni di ricovero a contatto con cateteri intravascolari o tubi endotracheali, può aumentare il rischio di infezione delle vie respiratorie e del flusso sanguigno..
La polmonite acquisita in ospedale è la più comune delle infezioni causate da A. baumanii. Comunemente contratta nelle Unità di Terapia Intensiva, da pazienti sottoposti a respirazione assistita meccanicamente.
A. baumanii ha anche causato gravi problemi di infezione al personale militare con traumi del dopoguerra, in particolare in Iraq e Afghanistan. In particolare, a causa di osteomielite e infezioni dei tessuti molli, che possono causare necrosi e cellulite.
Ci sono anche rischi di meningite da A. baumanii in pazienti che si stanno riprendendo da neurochirurgia.
Individui suscettibili alle infezioni da A. baumanii includere coloro che sono stati precedentemente sottoposti all'uso di antibiotici, interventi chirurgici importanti, ustioni, traumi, immunosoppressione o l'uso di dispositivi medici invasivi, principalmente ventilazione meccanica, in Unità di Terapia Intensiva.
Sintomi
Non esiste una sintomatologia specifica delle infezioni da A. baumanii. Ciascuna delle diverse infezioni prodotte da questo batterio ha i suoi sintomi caratteristici..
In generale i sintomi di infezioni che possono coinvolgere A. baumanii o altri batteri opportunisti come Klebsiella pneumoniae Y Streptococcus pneumoniae, può includere febbre, brividi, eruzione cutanea, minzione dolorosa, bisogno urgente di urinare frequentemente, confusione o stati mentali alterati, nausea, dolore muscolare, dolore toracico e tosse.
Trattamento
Antibiotici per trattare le infezioni da A. baumannii sono estremamente limitate, a causa della loro grande capacità di acquisire resistenze e multi-resistenze. Per questo motivo, è importante determinare la suscettibilità di ogni ceppo a diversi antibiotici per garantire l'efficacia di ogni trattamento..
Data la resistenza ai carbapenemi, si è fatto ricorso all'uso di polimixine, nello specifico della colistina, pur avendo un indice di resistenza relativamente basso e i suoi effetti collaterali sui reni.
Tuttavia, sono già stati rilevati ceppi resistenti alla colistina. In alternativa alla resistenza a questi antibiotici, è stata utilizzata la terapia combinata.
Riferimenti
- Bergogne-Bérézin, E. & Towner, K.J. Acinetobacter spp. come patogeni nosocomiali: caratteristiche microbiologiche, cliniche ed epidemiologiche. Clin Microbiol Rev, 9 (1996), pagg. 148-165.
- Fournier, P.E., Richet, H. (2006). L'epidemiologia e il controllo di Acinetobacter baumanii nelle strutture sanitarie. Malattie infettive cliniche, 42: 692-9.
- Hernández Torres, A., García Vázquez, E., Yagüe, G. &, Gómez Gómez, J. (2010) Acinetobacter baumanii Multiresistente: situazione clinica attuale e nuove prospettive Revista Española de Quimioterapia, 23 (1): 12-19.
- Maragakis LL, Perl TM. Acinetobacter baumanii: epidemiologia, resistenza antimicrobica e opzioni di trattamento. Clin Infec Dis 2008; 46: 1254-63.
- McConnell, M.j., Actis, L. & Pachón, J. (2013) Acinetobacter baumannii: infezioni umane, fattori che contribuiscono alla patogenesi e modelli animali. Recensioni di microbiologia FEMS, 37: 130-155.
- Peleg, A.Y., Seifert, H. & Paterson, D.L. (2008). Acinetobacter baumannii: comparsa di un agente patogeno di successo. Recensioni di microbiologia clinica, 21 (3): 538-82.
- Vanegas-Múnera, J.M., Roncancio-Villamil, G. & Jiménez-Quiceno, J.N. (2014). Acinetobacter baumannii: importanza clinica, meccanismi di resistenza e diagnosi. Rivista di medicina del CES, 28 (2): 233-246.



Nessun utente ha ancora commentato questo articolo.