
Struttura, caratteristiche, composti e derivati del gruppo acilico
Il gruppo acile È un frammento molecolare che in chimica organica è solitamente derivato da acidi carbossilici. La sua formula è RCO, dove R è un sostituente carbonio, alchile o arile, legato covalentemente e direttamente al gruppo carbonile, C = O. Di solito è solo una frazione della struttura di un composto organico, come una biomolecola..
Si dice che sia derivato da un acido carbossilico, RCOOH, perché sarà sufficiente eliminare il gruppo idrossile, OH, per ottenere il gruppo acile, RCO. Si noti che questo gruppo comprende un'ampia famiglia di composti organici (e inorganici). Questa famiglia è generalmente nota come composti acilici (e non asilo).

Nell'immagine in alto abbiamo la formula strutturale del gruppo acile. È facile riconoscerlo osservando una qualsiasi struttura molecolare, poiché si trova sempre alle estremità ed è indicato dal gruppo carbonile. Un esempio di questo lo vedremo nella molecola acetil-CoA, essenziale per il ciclo di Krebs.
L'incorporazione di questo gruppo in una molecola è nota come reazione di acilazione. Il gruppo acile fa parte della routine di lavoro nelle sintesi organiche.
Indice articolo
- 1 Struttura e caratteristiche del gruppo acile
- 2 Composti e derivati
- 2.1 - Cloruri
- 2.2 - Radicale
- 2.3 - Catione
- 2.4 - Amidi
- 2.5 - Aldeidi
- 2.6 - Chetoni ed esteri
- 2.7 - Commento generale
- 3 Esempi di gruppo acile
- 4 Riferimenti
Struttura e caratteristiche del gruppo acile
La struttura del gruppo acile dipende dall'identità di R. L'atomo di carbonio di detta catena laterale R, nonché il C = O a cui è attaccato, si trovano sullo stesso piano. Il segmento RCO della prima immagine è quindi piatto.
Tuttavia, questo fatto potrebbe sembrare insignificante se non fosse per le caratteristiche elettroniche di C = O: l'atomo di carbonio ha un leggero deficit di elettroni. Questo lo rende suscettibile all'attacco di agenti nucleofili, ricchi di elettroni. Pertanto, il gruppo acile è reattivo, essendo un sito specifico in cui vengono eseguite le sintesi organiche..
Composti e derivati
A seconda delle catene R o degli atomi che si trovano a destra di RCO, si ottengono diversi composti o derivati del gruppo acilico.
- Cloruri
Supponiamo ad esempio che un atomo di cloro sia posto a destra di RCO. Questa ora sostituisce quella sinuosità rappresentata nella prima immagine, rimanendo come: RCOCl. Abbiamo quindi alcuni derivati chiamati cloruri acilici.
Ora, cambiando l'identità di R in RCOCl, otteniamo diversi cloruri acilici:
-HCOCl, R = H, metanoil cloruro, composto drasticamente instabile
-CH3COCl, R = CH3, cloruro di acetile
-CH3CHDueCOCl, R = CHDueCH3, cloruro di propionile
-C6H5COCl, R = C6H5 (anello benzenico), cloruro di benzoile
Lo stesso ragionamento si applica ai fluoruri acilici, ai bromuri e agli ioduri. Questi composti vengono utilizzati nelle reazioni di acilazione, con lo scopo di incorporare RCO come sostituente di una molecola più grande; ad esempio, a un anello benzenico.
- Radicale
L'acile può esistere momentaneamente come un radicale, RCO •, originato da un'aldeide. Questa specie è molto instabile ed è immediatamente sproporzionata rispetto a un radicale alchilico e monossido di carbonio:
RC • = O → R • + C≡O
- Catione
Il gruppo acile può anche presentarsi come catione, RCO+, essendo un intermedio che reagisce per acilare una molecola. Questa specie contiene due strutture di risonanza rappresentate nell'immagine sottostante:
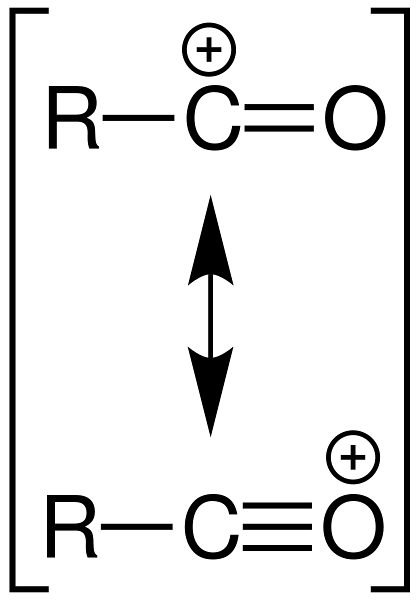
Nota come la carica parziale positiva viene distribuita tra gli atomi di carbonio e ossigeno. Di queste due strutture, [R-C≡O+], con la carica positiva sull'ossigeno, è il più predominante.
- Amides
Supponiamo ora che al posto di un atomo di Cl mettiamo un gruppo amminico, NHDue. Avremo quindi un'ammide, RCONHDue, RC (O) NHDue o RC = ONHDue. Quindi, cambiando finalmente l'identità di R, otterremo una famiglia di ammidi.
- Aldeidi
Se invece di NHDue posizioniamo un atomo di idrogeno, otterremo un'aldeide, RCOH o RCHO. Si noti che il gruppo acile è ancora presente anche quando è passato in secondo piano di importanza. Sia le aldeidi che le ammidi sono composti acilici.
- Chetoni ed esteri
Continuando con lo stesso ragionamento, possiamo sostituire H con un'altra catena laterale R, che darà origine a un chetone, RCOR 'o RC (O) R'. Questa volta il gruppo acile è più "nascosto", poiché una delle due estremità potrebbe essere considerata come RCO o R'CO.
D'altra parte, R 'può anche essere sostituito a OR', dando origine a un estere, RCOOR '. Negli esteri il gruppo acile è riconosciuto ad occhio nudo perché si trova sul lato sinistro del gruppo carbonile.
- Commento generale
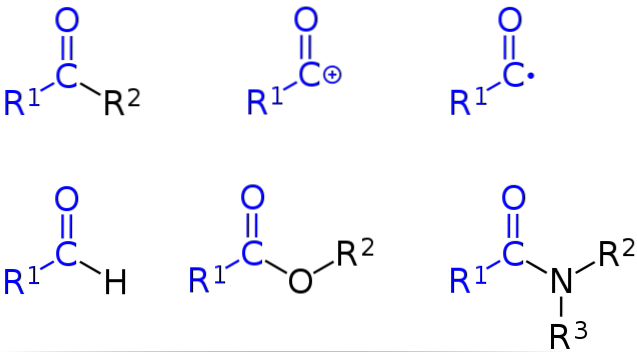
L'immagine in alto rappresenta globalmente tutto quanto discusso in questa sezione. Il gruppo acile è evidenziato in blu, e partendo dall'angolo superiore, da sinistra a destra, abbiamo: chetoni, catione acile, radicale acilico, aldeide, esteri e ammidi.
Sebbene il gruppo acile sia presente in questi composti, così come negli acidi carbossilici e nei tioesteri (RCO-SR '), al gruppo carbonile viene solitamente data maggiore importanza quando si definiscono i suoi momenti di dipolo. L'RCO è di maggiore interesse quando si trova come sostituente, o quando è direttamente collegato a un metallo (acili metallici).
A seconda del composto, RCO può avere nomi diversi, come si vede nella sottosezione sui cloruri acilici. Ad esempio, CH3La CO è nota come acetile o etanoile, mentre CH3CHDueCO, propionile o propanoile.
Esempi di gruppo acile

Uno degli esempi più rappresentativi di composti acilici è l'acetil-CoA (immagine in alto). Notare che viene immediatamente identificato perché evidenziato in blu. Il gruppo acile di acetil-CoA, come indica il nome, è acetile, CH3CO. Anche se può non sembrare, questo gruppo è essenziale nel ciclo di Krebs del nostro corpo.
Gli amminoacidi contengono anche il gruppo acile, solo che, ancora una volta, tende a passare inosservato. Ad esempio, per la glicina, NHDue‐CHDue‐COOH, il suo gruppo acile diventa il segmento NHDue‐CHDue‐CO e si chiama glicile. Nel frattempo, per la lisina, il suo gruppo acile diventa NHDue(CHDue)4CHNHDueCO, che si chiama lisile.
Sebbene di solito non sia discusso molto regolarmente, i gruppi acilici possono anche provenire da acidi inorganici; cioè, l'atomo centrale non deve essere carbonio, ma può anche essere composto da altri elementi. Ad esempio, un gruppo acile potrebbe anche essere RSO (RS = O), derivato dall'acido solfonico, o RPO (RP = O), derivato dall'acido fosfonico..
Riferimenti
- Morrison, R. T. e Boyd, R, N. (1987). Chimica organica. 5a edizione. Editoriale Addison-Wesley Interamericana.
- Carey F. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimica organica. (10a edizione.). Wiley plus.
- Wikipedia. (2020). Gruppo acilico. Estratto da: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (11 febbraio 2020). Definizione ed esempi del gruppo acilico. Estratto da: thoughtco.com
- Laura Foist. (2020). Acyl Group: definizione e struttura. Studia. Estratto da: study.com
- Steven A. Hardinger. (2017). Glossario illustrato di chimica organica: gruppo acilico. Estratto da: chem.ucla.edu


Nessun utente ha ancora commentato questo articolo.