
Struttura degli alcani lineari, proprietà, nomenclatura, esempi
Il alcani lineari sono idrocarburi saturi la cui formula chimica generale è n-CnH2n + 2. Poiché sono idrocarburi saturi, tutti i loro legami sono semplici (C-H) e sono composti solo da atomi di carbonio e idrogeno. Sono anche chiamate paraffine, differenziandole dagli alcani ramificati, che sono chiamati isoparaffine..
Questi idrocarburi mancano di rami e anelli. Più che linee, questa famiglia di composti organici è più simile a catene (alcano a catena lineare); o da un punto di vista culinario, agli spaghetti (crudi e cotti).

Gli spaghetti crudi arrivano a rappresentare lo stato ideale e isolato degli alcani lineari, sebbene con una spiccata tendenza alla rottura; mentre quelle cotte, al dente o meno, si avvicinano al loro stato naturale e sinergico: alcune interagiscono con altre in un insieme (il piatto di pasta, per esempio).
Questi tipi di idrocarburi si trovano naturalmente nel gas naturale e nei giacimenti petroliferi. Quelle più leggere presentano caratteristiche lubrificanti, mentre quelle pesanti si comportano come un asfalto indesiderabile; solubile, invece, in paraffine. Servono molto bene come solventi, lubrificanti, carburanti e asfalto.
Indice articolo
- 1 Struttura degli alcani lineari
- 1.1 Gruppi
- 1.2 Lunghezze delle vostre catene
- 1.3 Conformazioni
- 2 Proprietà
- 2.1 Fisico
- 2.2 Interazioni
- 2.3 Stabilità
- 3 Nomenclatura
- 4 esempi
- 5 Riferimenti
Struttura degli alcani lineari
Gruppi
È stato detto che la formula generale di questi alcani è CnH2n + 2. Questa formula infatti è la stessa per tutti gli alcani, lineari o ramificati. La differenza quindi nel n- che precede la formula per alcano, la cui denotazione significa "normale".
Si vedrà in seguito che questo n- non è necessario per alcani con un numero di carbonio uguale o inferiore a quattro (n ≤ 4).
Una linea o catena non può essere costituita da un singolo atomo di carbonio, quindi il metano (CH4, n = 1). Se n = 2, abbiamo etano, CH3-CH3. Si noti che questo alcano è costituito da due gruppi metilici, CH3, collegati insieme.
Aumentando il numero di atomi di carbonio, n = 3, si ottiene l'alcano propano, CH3-CHDue-CH3. Ora appare un nuovo gruppo, CHDue, chiamato metilene. Non importa quanto sia grande l'alcano lineare, avrà sempre solo due gruppi: CH3 e CHDue.
Lunghezze delle loro catene
Quando n o il numero di atomi di carbonio nell'alcano lineare aumenta, c'è una costante in tutte le strutture risultanti: il numero di gruppi metilenici aumenta. Ad esempio, supponiamo alcani lineari con n = 4, 5 e 6:
CH3-CHDue-CHDue-CH3 (n-butano)
CH3-CHDue-CHDue-CHDue-CH3 (n-pentano)
CH3-CHDue-CHDue-CHDue-CHDue-CH3 (n-esano)
Le catene si allungano perché aggiungono gruppi CH alle loro struttureDue. Pertanto, un alcano lineare lungo o corto differisce di quanti CHDue separa i due gruppi terminali CH3. Tutti questi alcani hanno solo due di questi CH3: all'inizio della stringa e alla fine di essa. Se ne avessi di più, implicherebbe la presenza di rami.
Allo stesso modo si nota la totale assenza di gruppi CH, presenti solo nei rami o quando sono presenti gruppi sostituenti legati ad uno degli atomi di carbonio della catena.
La formula strutturale può essere riassunta come segue: CH3(CHDue)n-2CH3. Prova ad applicarlo e ad illustrarlo.
Conformazioni
Alcuni alcani lineari possono essere più lunghi o più corti di altri. Stando così le cose, n può avere un valore di 2 a ∞; cioè una catena composta da infiniti gruppi CHDue e due gruppi CH3 terminali (teoricamente possibile). Tuttavia, non tutte le stringhe sono "sistemate" nello stesso modo nello spazio..
È qui che sorgono le conformazioni strutturali degli alcani. Cosa devono? Alla rotabilità dei legami C-H e alla loro flessibilità. Quando questi collegamenti ruotano o ruotano attorno a un asse internucleare, le catene iniziano a flettersi, piegarsi o avvolgersi, allontanandosi dalla loro caratteristica lineare originale..
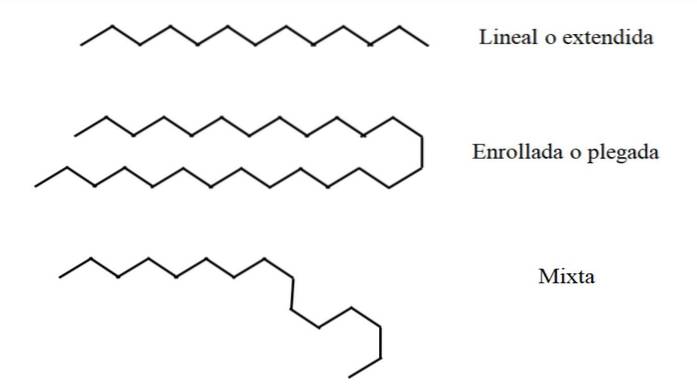
Lineare
Nell'immagine in alto, ad esempio, è mostrata in alto una catena a tredici atomi di carbonio che rimane lineare o estesa. Questa conformazione è ideale, poiché si presume che l'ambiente molecolare influenzi minimamente la disposizione spaziale degli atomi nella catena. Niente la disturba e non ha bisogno di piegarsi.
Arrotolato o piegato
Al centro dell'immagine, la catena a 27 atomi di carbonio subisce un disturbo esterno. La struttura, per essere più "confortevole", ruota le sue maglie in modo che si ripieghi su se stessa; proprio come un lungo spaghetto.
Studi computazionali hanno dimostrato che il numero massimo di atomi di carbonio che una catena lineare può avere è n = 17. Da n = 18, è impossibile che non inizi a piegarsi o avvolgersi.
Misto
Se la catena è molto lunga, potrebbero esserci regioni della catena che rimangono lineari mentre altre sono state piegate o avvolte. Di tutte, questa è forse la conformazione più vicina alla realtà.
Proprietà
Fisico
Essendo idrocarburi, sono essenzialmente apolari, e quindi idrofobici. Ciò significa che non possono mescolarsi con l'acqua. Non sono molto densi perché le loro catene lasciano troppi spazi vuoti tra di loro.
Allo stesso modo, i loro stati fisici vanno da gassosi (per n < 5), líquidos (para n < 13) o sólidos (para n ≥ 14), y dependen de la longitud de la cadena.
Interazioni
Le molecole degli alcani lineari sono apolari e quindi le loro forze intermolecolari sono del tipo di diffusione di Londra. Le catene (che probabilmente assumono una conformazione mista), vengono poi attratte dall'azione delle loro masse molecolari e dei dipoli indotti istantaneamente dei loro atomi di idrogeno e carbonio..
È per questo motivo che quando la catena diventa più lunga, e quindi più pesante, i suoi punti di ebollizione e di fusione aumentano allo stesso modo..
Stabilità
Più lunga è la catena, più è instabile. Generalmente rompono i loro collegamenti per creare catene più piccole da una grande. In effetti, questo processo è noto come cracking, molto utilizzato nella raffinazione del petrolio.
Nomenclatura
Per nominare gli alcani lineari, aggiungi semplicemente l'indicatore n prima del nome. Se n = 3, come con il propano, è impossibile che questo alcano presenti qualsiasi ramificazione:
CH3-CHDue-CH3
Cosa che non accade dopo n = 4, cioè con n-butano e gli altri alcani:
CH3-CHDue-CHDue-CH3
O
(CH3)DueCH-CH3
La seconda struttura corrisponde all'isobutano, che consiste in un isomero strutturale del butano. Per differenziarli l'uno dall'altro, entra in gioco l'indicatore n-. Quindi, il n-butano si riferisce solo all'isomero lineare, senza rami.
Più alto è n, maggiore è il numero di isomeri strutturali e più importante sarà usare n- per riferirsi all'isomero lineare.
Ad esempio, ottano, C8H18 (C8H8 × 2 + 2), ha fino a tredici isomeri strutturali, poiché sono possibili molti rami. L'isomero lineare, tuttavia, è chiamato: n-ottano, e la sua struttura è:
CH3-CHDue-CHDue-CHDue-CHDue-CHDue-CHDue-CH3
Esempi
Sono menzionati di seguito e per finire alcuni alcani lineari:
-Etano (CDueH6): CH3CH3
-Propano (C3H8): CH3CHDueCH3
-n-Eptano (C7H16): CH3(CHDue)5CH3.
- n-Dean (C10H22): CH3(CHDue)8CH3.
-n-Esadecano (C16H3. 4): CH3(CHDue)14CH3.
-n-Nonadecano (C.19H40): CH3(CHDue)17CH3.
-n-Eicosane (CventiH42): CH3(CHDue)18CH3.
- n-Ettano (C.100H202): CH3(CHDue)98CH3.
Riferimenti
- Carey F. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison, R. T. e Boyd, R, N. (1987). Chimica organica. (5a edizione). Editoriale Addison-Wesley Interamericana.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimica organica. Ammine. (10a edizione.). Wiley plus.
- Jonathan M. Goodman. (1997). Qual è l'alcano non ramificato più lungo con una conformazione minima globale lineare? J. Chem. Inf. Comput. Sci. 1997, 37, 5, 876-878.
- Garcia Nissa. (2019). Cosa sono gli alcani? Studia. Estratto da: study.com
- Sig. Kevin A. Boudreaux. (2019). Alcani. Estratto da: angelo.edu
- Elenco degli alcheni a catena lineare. [PDF]. Recupero da: laney.edu
- Helmenstine, Anne Marie, Ph.D. (7 settembre 2018). Assegna un nome ai primi 10 alcani. Estratto da: thoughtco.com
- Scienza eccentrica. (20 marzo 2013). Alcani a catena lineare: proprietà predittive. Estratto da: quirkyscience.com
- Wikipedia. (2019). Alcani superiori. Estratto da: en.wikipedia.org



Nessun utente ha ancora commentato questo articolo.