
30 reazioni chimiche della vita quotidiana
Il reazioni chimiche possiamo trovarli nella vita di tutti i giorni in modo generale. Questa è la risposta che un chimico potrebbe darti senza che sbagli a esagerare. Ad esempio, quando un fiammifero brucia, si verifica una reazione di combustione.
Ed è che qualcuno desideroso di questa materia proverà a vedere le cose dal punto di vista molecolare o atomico, proverà a vedere reazioni ovunque e le molecole si trasmutano costantemente.

Le persone esperte di chimica non possono fare a meno di vedere le cose da questo punto di vista, proprio come un fisico potrebbe vedere le cose da un punto di vista nucleare o un biologo da un punto di vista cellulare..
Per giustificare il commento, ecco 30 esempi di chimica presenti nella vita di tutti i giorni. Sono reazioni chimiche che passano inosservate a casa, in cucina, in giardino, per strada o addirittura all'interno del nostro corpo. Spero con questo di dare luce alla solita e routine che è la chimica nella quotidianità.
Reazioni chimiche che vedi ogni giorno nella tua vita
Chimica in cucina
1- Reazioni di solvibilità: quando il sale si scioglie in acqua, i legami ionici si rompono, producendo una solvatazione di cationi e anioni.
NaCl → Na+ + Cl-
Tecnicamente viene preparata una soluzione di cloruro di sodio in acqua.
2- Cambiamenti di fase: quando l'acqua viene bollita durante la cottura o la preparazione del caffè o del tè, si verifica un cambio di fase tra l'acqua liquida e l'acqua gassata.
HDueO(l) → HDueO(g)
3- Reazioni di combustione- Le cucine a gas utilizzano propano per produrre una fiamma.
C3H8 + 5ODue → 3CODue + 4HDueO
4- Cloro: Il cloro utilizzato come detergente è in realtà clorito di sodio che è un agente riducente. Le macchie sui vestiti sono chiamate cromofori e hanno insaturazioni. Il cloro attacca queste insaturazioni rimuovendo il colore dalle macchie. Tecnicamente non rimuove la macchia ma la rende invisibile.
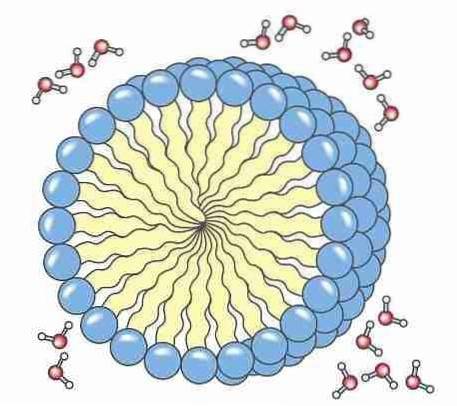
5- Il sapone: saponi e detergenti hanno una parte polare, solitamente un acido carbossilico, attaccata ad una catena alifatica non polare che gli conferisce la capacità di formare micelle. Queste micelle hanno la capacità di circondare lo sporco in modo che possa essere rimosso da vestiti, piatti e dal nostro corpo..
6- Bicarbonato di sodio: è una base debole che reagendo con acidi come l'aceto o l'acqua (che è leggermente acida) rilascia anidride carbonica.
NaHCO3 + CH3COOH → CH3COONa + HDueO + CODue
Questo composto è l'ingrediente attivo di molti antiacidi..
7- Medio termineLa cottura è un cambiamento chimico che altera il cibo per renderlo più saporito, uccidere i microrganismi pericolosi e renderlo più digeribile.
Il calore della cottura può denaturare le proteine, promuovere reazioni chimiche tra gli ingredienti, caramellare gli zuccheri, ecc..
8- Aroma e colore artificiali: molti alimenti trasformati contengono sostanze chimiche che conferiscono loro un sapore o un colore specifico e aiutano a preservarli.
9- Piangi per la cipolla: la cipolla contiene molecole di amminoacidi solfossidi. Quando la cipolla viene tagliata, le pareti cellulari si rompono rilasciando questi solfossidi insieme ad enzimi che la scompongono in acidi solfenici, un composto organosolforico di formula R-SOH che è irritante per gli occhi..
Chimica a casa
10- Batterie: utilizzano reazioni elettrochimiche o redox per convertire l'energia chimica in energia elettrica. Le reazioni redox spontanee si verificano nelle cellule galvaniche, mentre le reazioni chimiche non spontanee si verificano nelle cellule elettrolitiche..
11- Schermi LCD: I televisori LCD contengono molecole di cristalli elicoidali che hanno la proprietà di orientarsi secondo un segnale elettrico e di fargli cambiare la tonalità o il colore fornito da una lampadina a LED. Ogni molecola di cristallo rappresenta un pixel sul televisore, maggiore è il numero di molecole, maggiore è la risoluzione..
12- Vecchi libri che hanno un buon profumo: la decomposizione della cellulosa della carta dei libri, dona quel colore giallastro alle foglie e un odore di vaniglia. Se hai vecchi libri che hanno un buon odore nella tua biblioteca è dovuto alle molecole di lignina o vanillina che contengono..
13- Farmaci e droghe: alcuni farmaci sono molecole che bloccano parzialmente l'attività ormonale prodotta da un determinato stimolo (ad esempio farmaci antiepilettici) mentre altri sono inibitori enzimatici, come ad esempio antidolorifici.

14- Shampoo: come detergenti e saponi, gli shampoo rimuovono l'olio dal cuoio capelluto formando micelle. L'ingrediente che si prende cura di questo è solitamente solfati come sodio o ammonio dodecil solfato o lauril etere solfato..
15- Deodoranti e antitraspiranti: il cattivo odore di ascelle, piedi e alito è prodotto da batteri che si nutrono delle proteine e dei grassi del sudore secreti dalle ghiandole apocrine.
I deodoranti hanno un composto chimico chiamato triclosan che è un potente antibatterico e fungicida. D'altra parte, gli antitraspiranti hanno sali di alluminio che penetrano nei pori e prevengono la sudorazione..
16- Cosmetici e trucco: sono sostanze chimiche e pigmenti che aderiscono alla pelle. Di solito sono composti non polari come cere e oli.
Chimica in giardino
17- Fotosintesi: è il processo mediante il quale le piante verdi producono il proprio cibo. Ciò si verifica in presenza di luce solare e altre materie prime, vale a dire anidride carbonica e acqua. Il pigmento della clorofilla raccoglie l'energia luminosa dalla luce solare, che viene convertita in glucosio.
6CODue+ 6HDueO + hν → C6H12O6 + 6 °Due
18- Reazioni di ossidazione- Si nota spesso un rivestimento di ruggine sulle superfici in ferro non verniciate che porta gradualmente alla disgregazione del ferro. Questo è un fenomeno chimico chiamato ossidazione..
In questo caso, il ferro si combina con l'ossigeno in presenza di acqua, portando alla formazione di ossidi di ferro..
Fede + ODue + HDueO → FedeDueO3. XHDueO
19- decomposizione organica: la decomposizione del cibo organico o anche degli esseri viventi sono reazioni di ossidazione prodotte da batteri che degradano le macromolecole biochimiche in molecole semplici come nitriti, nitrati, CODue e acqua.

20- Fertilizzanti: potassio, nitrati, fosfati e solfati sono utilizzati nei terreni per fornire nutrienti alle piante e sono in grado di crescere.
21- Pesticidi: sono sostanze chimiche utilizzate per fumigare colture o giardini. Di solito sono neurotossine che colpiscono i batteri o gli insetti che consumano i raccolti.
Chimica in strada
22- Combustione di benzina: le auto utilizzano la benzina come carburante attraverso esplosioni controllate che muovono i pistoni dei motori.
23- Fumo dalle auto: produce radicali liberi che sono composti molto reattivi e attaccano la pelle oi capelli, rendendoli secchi e fragili, senza contare che sono cancerogeni.
24- Pioggia acida: l'eccesso di ossidi di zolfo e di azoto nell'atmosfera prodotto da fabbriche e automobili si dissolve nell'acqua delle nuvole producendo acido solforoso, solforico e nitrico che precipita sotto forma di pioggia acida.

25- Costruzioni: Il cemento e altri materiali utilizzati nella costruzione di case come pitture, intonaco e molti altri sono i prodotti della chimica. In particolare, il cemento è costituito da molecole di idrossido di calcio, chiamate anche calce viva..
Chimica nel tuo corpo
26- Digestione del cibo- La digestione si basa su reazioni chimiche tra cibo e acidi ed enzimi per scomporre le molecole in nutrienti che il corpo può assorbire e utilizzare.
27- Respirazione aerobica: il principale processo che produce energia nell'organismo è la glicolisi aerobica. Qui, la respirazione aiuta a scomporre il glucosio (una fonte di energia) in acqua, anidride carbonica ed energia sotto forma di ATP. C6H12O6 + 6 °Due → 6CODue + 6HDueO + Energy (36 ATP)
28- Respirazione anaerobica: A causa dell'eccessivo esercizio fisico, a volte le nostre cellule del corpo esauriscono l'ossigeno e respirano in modo anaerobico. Ciò provoca la sintesi dell'acido lattico. La respirazione anaerobica è presente in alcuni batteri, lieviti e altri organismi. L'equazione della respirazione anaerobica è:
C6H12O6 → 2C3H6O3 + Energia (2ATP)
29- Movimento muscolare: la tensione o il rilassamento dei muscoli è dovuto ai cambiamenti conformazionali delle proteine del muscolo scheletrico. Questi cambiamenti sono prodotti grazie alla fosfocreatina, che perdendo un fosfato rilascia energia per il processo.

30- Pensiero: è un processo biochimico complesso dove la differenza di potenziale ionico crea gli impulsi elettrici dei neuroni.
Riferimenti
- Ali, A. (2013, 20 aprile). reazione chimica nella nostra vita quotidiana. Recupero da meritnation: meritnation.com.
- , G. (2015, 27 dicembre). Quali sono alcuni esempi di reazioni chimiche nella vita di tutti i giorni? Recuperato da socratic.org.
- Reazioni chimiche nella vita quotidiana. (2016, 3 agosto). Recupero da buzzle.com.
- Crystal, M. (2017, 25 aprile). Come vengono utilizzate le reazioni di riduzione dell'ossidazione nella vita quotidiana? Recuperato da sciencing.com.
- Helmenstine, A. (2015, 15 agosto). Quali sono alcuni esempi di chimica nella vita quotidiana? Estratto da sciencenotes.org.
- Helmenstine, A. M. (2017, 28 marzo). 10 esempi di reazioni chimiche nella vita quotidiana. Recuperato da thoughtco.com.
- Helmenstine, A. M. (2017, 29 marzo). Esempi di cambiamenti chimici. Recuperato da thoughtco.com.
- Reazioni. (2016, 7 giugno). Perché le cipolle ti fanno piangere? . Recuperato da youtube.com.



Nessun utente ha ancora commentato questo articolo.